Evaluar la validez del Conjunto Mínimo Básico de Datos (CMBD) para identificar anomalías congénitas mayores en la Comunitat Valenciana.
MétodosSe realizó un estudio epidemiológico retrospectivo. Del CMBD se seleccionaron las altas en menores de un año nacidos en 2007, residentes en la Comunitat Valenciana con código de anomalía congénita (740-759 CIE9-MC) y una muestra aleatoria de menores de un año sin altas con estos códigos. Tras revisar la documentación clínica, se clasificaron como verdaderos positivos y negativos y falsos positivos y negativos. Se calcularon el valor predictivo positivo y negativo y la sensibilidad. Se analizaron la concordancia de los diagnósticos entre el CMBD y la documentación clínica utilizando la prueba kappa.
ResultadosSe identificaron 2305 altas de 1651 pacientes. En los 544 pacientes de la muestra, 4 tenían alguna anomalía congénita mayor. El valor predictivo positivo fue del 56,4% (intervalo de confianza del 95% [IC95%]: 53,9-58,8) y el negativo fue del 99,3% (IC95%: 98,6-100,0). La sensibilidad del CMBD fue del 68,6% (IC95%: 66,1-71,1). Los códigos más frecuentes en los verdaderos positivos fueron: 745.5 (Comunicación interauricular), 745.4 (Comunicación interventricular) y 747.0 (Ductus arterioso persistente), y en los falsos positivos: 747.0, 745.5 y 752.51 (Criptorquidia). El 25,5% de los diagnósticos con anomalía congénita del CMBD no estaban en la historia clínica. Considerando todos los diagnósticos codificados en el CMBD, la concordancia fue de 0,70 (IC95%: 0,68-0,72).
ConclusionesEl CMBD es la principal fuente de información para la identificación de casos para el Registro Poblacional de Anomalías Congénitas de la Comunitat Valenciana, pero su principal limitación es el elevado número de casos falsos positivos que detecta.
To assess the validity of the Spanish Minimum Basic Data Set (MBDS) for identifying major congenital anomalies in the Valencian Community.
MethodsA retrospective epidemiological study was carried out. Children under the age of one year, born in 2007 and residing in the Valencian Community with congenital anomalies code 740-759 CIE9-MC, were selected from the MBDS, in addition to a random sample of children under the age of 1 year without these discharge codes. Having reviewed the clinical documentation, the cases were classified as true positives and negatives and false positives and negatives. Positive and negative predictive value and sensitivity were calculated. The kappa test was applied to analyse diagnostic consistency between the MBDS and the clinical documentation.
ResultsA total of 2305 discharges of 1651 patients were identified. 4 out of the 5434 patients sampled had a major congenital abnormality. The positive predictive value was 56.4% (95% confidence interval [95%CI]: 53.9-58.8) and the negative predictive value was 99.3% (95%CI: 98.6-100.0). MBDS sensitivity was 68.6% (95%CI: 66.1-71.1). The most common codes in the true positives were: 745.5 (atrial septal defect), 745.4 (ventricular septal defect) and 747.0 (patent ductus arteriosus) and in the false positives: 747.0, 745.5 and 752.51 (cryptorchidism). 25.5% of diagnoses with congenital anomaly from the MBDS were not in the clinical documentation. Considering all diagnoses coded in the MBDS, the correlation was 0.70 (95%CI: 0.68-0.72)
ConclusionsThe MBDS is the main source of information to detect cases in the registry of congenital anomalies of the Valencian Community. Its main limitation is the high number of false positive cases detected.
La Organización Mundial de la Salud (OMS) define las anomalías congénitas como «toda anomalía del desarrollo morfológico, estructural, funcional o molecular presente al nacer, externa o interna, familiar o esporádica, hereditaria o no, única o múltiple». Son diagnosticadas principalmente en el periodo prenatal, al nacimiento o en el primer año de vida1,2.
Representan un importante problema de salud pública en términos de impacto en calidad de vida de pacientes y familiares, de contribución a la mortalidad fetal e infantil y de coste emocional, médico, social y educacional necesario para mejorar la calidad de vida1.
La OMS estima que en 2012 fueron la causa de unas 302.000 muertes neonatales en el mundo y de 337 en España3. En la Unión Europea, las 5233 defunciones por anomalías congénitas registradas en 2012 representaron la cuarta parte de las ocurridas en el primer año de vida. Esta proporción en España fue del 22,2% (312 fallecimientos)4,5.
En la Comunitat Valenciana, son la segunda causa de mortalidad en menores de un año. En 2012 se registraron 32 defunciones por anomalías congénitas (25,2% de las ocurridas en el primer año de vida)6.
La prevalencia en la Unión Europea de anomalías congénitas mayores para el periodo 2004-2008 fue de 233,4/10.000 nacimientos7.
La etiología de la mayoría de las anomalías congénitas es desconocida, pero se sospecha que interaccionan múltiples factores ambientales y genéticos. El 15% son identificadas como anomalías cromosómicas. Menos del 5% de los casos son atribuidos a una mutación de un gen conocido y menos del 5% a una exposición a un teratógeno ambiental1,8.
El crecimiento industrial, la introducción en el ambiente de nuevos contaminantes y la participación activa de la mujer en el mundo laboral conllevan un potencial aumento del riesgo de alteraciones por factores ambientales, que hace necesario el desarrollo de sistemas de información como base para la vigilancia y la investigación epidemiológica de las anomalías congénitas y para la evaluación de intervenciones sanitarias7,9,10.
Con esta finalidad se creó The European Surveillance of Congenital Anomalies (EUROCAT), una red de registros poblacionales de anomalías congénitas con una metodología estandarizada que cubre 1,7 millones de nacimientos de la UE7,11 y de la que forma parte el Registro Poblacional de Anomalías Congénitas de la Comunitat Valenciana (RPAC-CV) desde el año 2011.
Dado el alto coste de la recogida de datos primarios y la limitación de recursos, la utilización de fuentes de datos administrativos ha demostrado ser una valiosa fuente de información en el ámbito de la salud pública12,13.
En España, el Consejo Interterritorial aprobó el Conjunto Mínimo Básico de Datos (CMBD) en 198714. Se creó con la finalidad de facilitar los procesos de gestión hospitalaria, implantación de sistemas de financiación, elaboración de indicadores y control de calidad asistencial, y también proporciona información para investigación clínica y epidemiologíca14. La principal limitación fue la calidad de los datos, clínicos y de residencia15, pero con el tiempo ha habido una mejora progresiva y ha sido utilizado por diversos investigadores16,17. Las altas hospitalarias también han sido utilizadas en salud materno-infantil18,19, en vigilancia de anomalías congénitas20–22 y como fuente de información de registros de anomalías congénitas23–25.
La exhaustividad para la identificación de anomalías congénitas y la validez de diagnósticos de altas hospitalarias han mostrado una gran variabilidad entre diferentes estudios, explicada probablemente por la metodología utilizada, las anomalías congénitas incluidas en el análisis y por el momento y el lugar en que fue realizado el estudio. Calle y Khoury26 observaron que un 49% de las anomalías congénitas no estaban en las altas hospitalarias al compararlas con los certificados de nacimiento. La sensibilidad de las altas hospitalarias obtenida por Ford et al.18 para las anomalías congénitas mayores fue de un 95,1% (intervalo de confianza del 95% [IC95%]: 83,5-99,4). Y un trabajo27 en la Comunitat Valenciana sobre la validez de diagnósticos informatizados en CMBD de anomalías congénitas, utilizando como referencia la información de las historias clínicas, mostró una sensibilidad del 64% y unos valores predictivos positivo y negativo superiores al 90%.
Considerando que el CMBD es una de las principales fuentes de información de registros poblacionales de anomalías congénitas24, y los problemas en la calidad de los datos identificada27, se planteó este estudio cuyo objetivo general es evaluar la validez del CMBD para identificar anomalías congénitas mayores (malformaciones que implican un riesgo vital, cirugía o secuelas graves) en menores de un año nacidos en 2007 residentes en la Comunitat Valenciana, tomando como referencia la información procedente de las historias de los servicios de neonatología de 10 hospitales públicos de la Comunitat Valenciana.
MétodoSe realizó un estudio epidemiológico observacional retrospectivo cuya población de referencia fue los nacidos en 2007 residentes en la Comunitat Valenciana con al menos un alta hospitalaria durante el primer año de vida en alguno de los 10 hospitales incluidos.
Las fuentes de información utilizadas fueron el CMBD de 2007-2008 de los 10 hospitales (4 en Alicante, 2 en Castellón y 4 en Valencia, incluyendo los hospitales de referencia de cada provincia y el de referencia de la Comunitat Valenciana para estas patologías), las historias y la documentación clínica de esos hospitales, y el RPAC-CV.
Respecto a las variables estudiadas, del CMBD se obtuvieron el número de tarjeta sanitaria (SIP), número de historia clínica, código de hospital, fecha de nacimiento, sexo, residencia, fecha de ingreso y de alta, diagnósticos principal y secundarios y circunstancia del alta.
A partir de las variables anteriores se obtuvieron la edad al ingreso, el número de altas, las defunciones hospitalarias, el número de diagnósticos (suma de los diferentes diagnósticos de la anomalía congénita del paciente) y la codificación del diagnóstico principal con un código de anomalía congénita (mediante el cual se obtuvo una variable binaria según la presencia o no de un código de anomalía congénita en el diagnóstico principal de cualquiera de las altas).
Se definió caso como «paciente nacido en 2007, residente en la Comunitat Valenciana y con al menos un alta durante el primer año de vida en alguno de los hospitales participantes en la que el diagnóstico principal y/o alguno de los secundarios estuviera codificado como anomalía congénita mayor (definida por EUROCAT)».
A partir del CMBD de los hospitales incluidos correspondiente a 2007-2008 se seleccionaron las altas en menores de un año nacidos en el año 2007 en las que, al menos, el diagnóstico principal o los secundarios estuvieran codificados como anomalía congénita (códigos 740-759 de la Clasificación Internacional de Enfermedades 9a revisión-Modificación Clínica [CIE9-MC]).
Para valorar las altas con casos de las anomalías congénitas que fueran falsos negativos (FN), se seleccionó, utilizando los mismos CMBD que para los casos, una muestra de menores de un año nacidos en 2007 y residentes en la Comunitat Valenciana con al menos un alta hospitalaria en que ninguno de los diagnósticos incluyera un código de anomalía congénita. La selección de la muestra se llevó a cabo mediante muestreo aleatorio simple. Para calcular el tamaño de la muestra se consideró un nivel de confianza del 95%, una proporción de anomalías congénitas del 16%27 y una precisión del 3%, y se obtuvo una muestra total de 544 pacientes. Se amplió a 640 pacientes (15% pérdidas esperadas) para la obtención de reservas.
Tras la agrupación de las altas de cada paciente mediante el SIP, se revisaron las historias clínicas (referencia) en colaboración con los servicios de neonatología, tanto de casos de anomalía congénita como de la muestra. Los diagnósticos de anomalía congénita de la historia fueron codificados con la CIE9-MC.
Al comparar la información del CMBD y de las historias, se clasificaron los pacientes como verdaderos positivos (VP) cuando tenían al menos un diagnóstico de anomalía congénita mayor en ambas fuentes, falsos positivos (FP) cuando el diagnóstico de anomalía congénita mayor sólo estaba en el CMBD, FN cuando el diagnóstico de anomalía congénita mayor sólo estaba en la historia, y verdaderos negativos (VN) cuando los de la muestra no tenían registrado ningún diagnóstico de anomalía congénita mayor. Se compararon las características demográficas y clínicas de los casos VP y FP mediante la prueba de ji al cuadrado de Pearson.
El valor predictivo positivo (VPP) global se calculó como el cociente entre los casos VP y el total de casos identificados por el CMBD como anomalía congénita, y por hospitales. El valor predictivo negativo (VPN) se obtuvo como el cociente entre los VN obtenidos a partir de la muestra y el total de casos de esta. Se calcularon los IC95%.
La sensibilidad, junto con su IC95%, fue calculada como el cociente entre los casos VP identificados del CMBD y los casos de anomalías congénitas mayores incluidos en el RPAC-CV.
Para analizar la concordancia entre los diagnósticos a 3 dígitos procedentes del CMBD y los obtenidos de las historias, se aplicó la prueba de concordancia kappa y su IC95%. Para realizar todos los análisis se utilizó el programa EPIDAT 4.1.
ResultadosDel CMBD de 2007-2008 se identificaron 16.453 altas de menores de un año nacidos en 2007, de las que 2829 (17,2%) tenían algún diagnóstico como anomalía congénita. De estas, el 96,1% (2719) correspondían a pacientes residentes en la Comunitat Valenciana. Se analizaron 2305 altas (84,8% del total de altas de menores de un año nacidos en 2007 con al menos un código de anomalía congénita y residentes en la Comunitat Valenciana) procedentes de los hospitales incluidos, que representaban a un total de 1651 pacientes. En 33 de esos pacientes la documentación clínica no estaba disponible, por lo que finalmente en el análisis se incluyeron 1618 pacientes (el 98,0%) con algún código de anomalía congénita.
La revisión de las historias clínicas confirmó que 912 pacientes (56,4%) tenían al menos una anomalía congénita mayor (VP). En 706 casos (43,6%) no se identificó ninguna anomalía congénita mayor (FP).
De los 544 pacientes de la muestra, en 17 (3,1%) no estaba disponible la información clínica y se sustituyeron por 17 reservas. En la revisión de las historias se identificó que 4 (0,74%) pacientes tenían cada uno de ellos una anomalía congénita mayor, y por tanto se clasificaron como FN. Las anomalías congénitas incluidas en la historia y no detectadas por el CMBD fueron hipospadias, comunicación interventricular, atresia y estenosis de esófago y fisura palatina. Todos los casos FN de la muestra se identificaron en el mismo hospital.
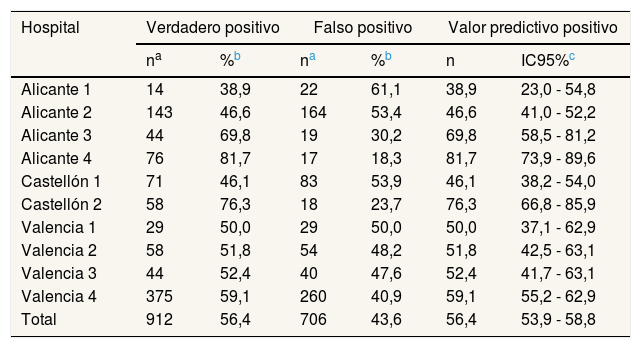
El VPP para el conjunto de los hospitales fue del 56,4% (IC95%: 53,9-58,8) y el VPN de 99,3% (IC95%: 98,6-100,0). El VPP para los diferentes hospitales se presenta en la tabla 1. Se observa que los hospitales con menor VPP, 38,9% (IC95%:23,0-54,8) y mayor VPP, 81,7% (IC95%: 73,9-89,6) están en la provincia de Alicante.
Distribución de los casos verdaderos positivos, falsos positivos, valor predictivo positivo y su intervalo de confianza al 95% por hospitales
| Hospital | Verdadero positivo | Falso positivo | Valor predictivo positivo | |||
|---|---|---|---|---|---|---|
| na | %b | na | %b | n | IC95%c | |
| Alicante 1 | 14 | 38,9 | 22 | 61,1 | 38,9 | 23,0 - 54,8 |
| Alicante 2 | 143 | 46,6 | 164 | 53,4 | 46,6 | 41,0 - 52,2 |
| Alicante 3 | 44 | 69,8 | 19 | 30,2 | 69,8 | 58,5 - 81,2 |
| Alicante 4 | 76 | 81,7 | 17 | 18,3 | 81,7 | 73,9 - 89,6 |
| Castellón 1 | 71 | 46,1 | 83 | 53,9 | 46,1 | 38,2 - 54,0 |
| Castellón 2 | 58 | 76,3 | 18 | 23,7 | 76,3 | 66,8 - 85,9 |
| Valencia 1 | 29 | 50,0 | 29 | 50,0 | 50,0 | 37,1 - 62,9 |
| Valencia 2 | 58 | 51,8 | 54 | 48,2 | 51,8 | 42,5 - 63,1 |
| Valencia 3 | 44 | 52,4 | 40 | 47,6 | 52,4 | 41,7 - 63,1 |
| Valencia 4 | 375 | 59,1 | 260 | 40,9 | 59,1 | 55,2 - 62,9 |
| Total | 912 | 56,4 | 706 | 43,6 | 56,4 | 53,9 - 58,8 |
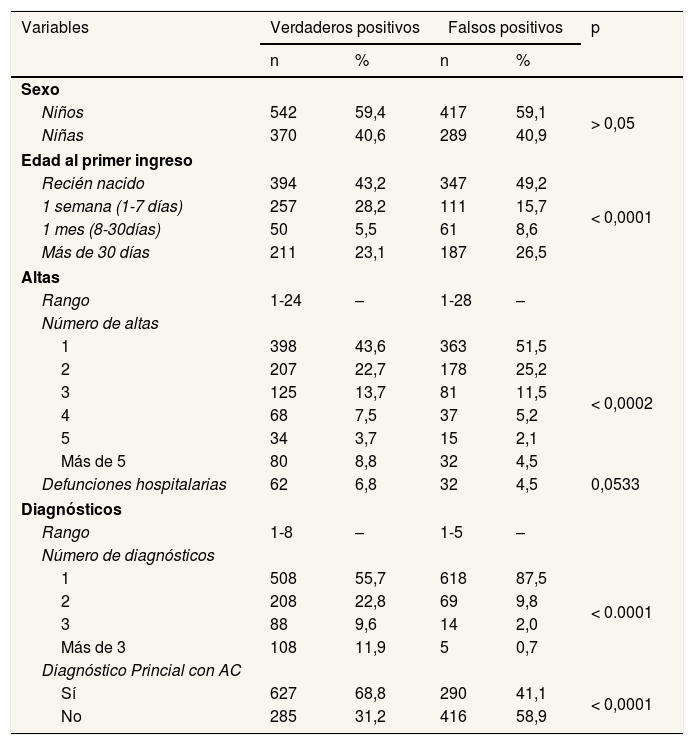
En la tabla 2 se presentan las características demográficas y clínicas de los VP y FP. Mientras que no hay diferencia significativa en la distribución de los VP y FP por sexo, para el resto de variables estudiadas la distribución es diferente. Así, la proporción de niños con alguna anomalía congénita detectada al nacer es mayor en los FP que en los VP, mientras que ocurre al contrario cuando la primera alta por anomalía congénita se produce entre el primer día de nacimiento y el séptimo. Por otro lado, si bien el rango del número de altas es más amplio en los FP, la proporción de casos con tres o más altas es superior en los VP. También la proporción de casos con mortalidad hospitalaria es superior en los VP. La proporción de casos con diagnóstico principal de anomalía congénita y el número de diagnósticos de diferentes anomalías congénitas son también superiores en los VP.
Características demográficas y clínicas de los casos verdaderos positivos y falsos positivos identificados a partir del CMBD
| Variables | Verdaderos positivos | Falsos positivos | p | ||
|---|---|---|---|---|---|
| n | % | n | % | ||
| Sexo | |||||
| Niños | 542 | 59,4 | 417 | 59,1 | > 0,05 |
| Niñas | 370 | 40,6 | 289 | 40,9 | |
| Edad al primer ingreso | |||||
| Recién nacido | 394 | 43,2 | 347 | 49,2 | < 0,0001 |
| 1 semana (1-7 días) | 257 | 28,2 | 111 | 15,7 | |
| 1 mes (8-30días) | 50 | 5,5 | 61 | 8,6 | |
| Más de 30 días | 211 | 23,1 | 187 | 26,5 | |
| Altas | |||||
| Rango | 1-24 | – | 1-28 | – | |
| Número de altas | |||||
| 1 | 398 | 43,6 | 363 | 51,5 | < 0,0002 |
| 2 | 207 | 22,7 | 178 | 25,2 | |
| 3 | 125 | 13,7 | 81 | 11,5 | |
| 4 | 68 | 7,5 | 37 | 5,2 | |
| 5 | 34 | 3,7 | 15 | 2,1 | |
| Más de 5 | 80 | 8,8 | 32 | 4,5 | |
| Defunciones hospitalarias | 62 | 6,8 | 32 | 4,5 | 0,0533 |
| Diagnósticos | |||||
| Rango | 1-8 | – | 1-5 | – | |
| Número de diagnósticos | |||||
| 1 | 508 | 55,7 | 618 | 87,5 | < 0.0001 |
| 2 | 208 | 22,8 | 69 | 9,8 | |
| 3 | 88 | 9,6 | 14 | 2,0 | |
| Más de 3 | 108 | 11,9 | 5 | 0,7 | |
| Diagnóstico Princial con AC | |||||
| Sí | 627 | 68,8 | 290 | 41,1 | < 0,0001 |
| No | 285 | 31,2 | 416 | 58,9 | |
AC: anomalía congénita.
La sensibilidad del CMBD para el conjunto de hospitales fue del 68,6% (IC95%: 66,1-71,1), tomando como denominador los 1330 casos de anomalías congénitas mayores registradas para los menores de un año nacidos en 2007 en el RPAC-CV.
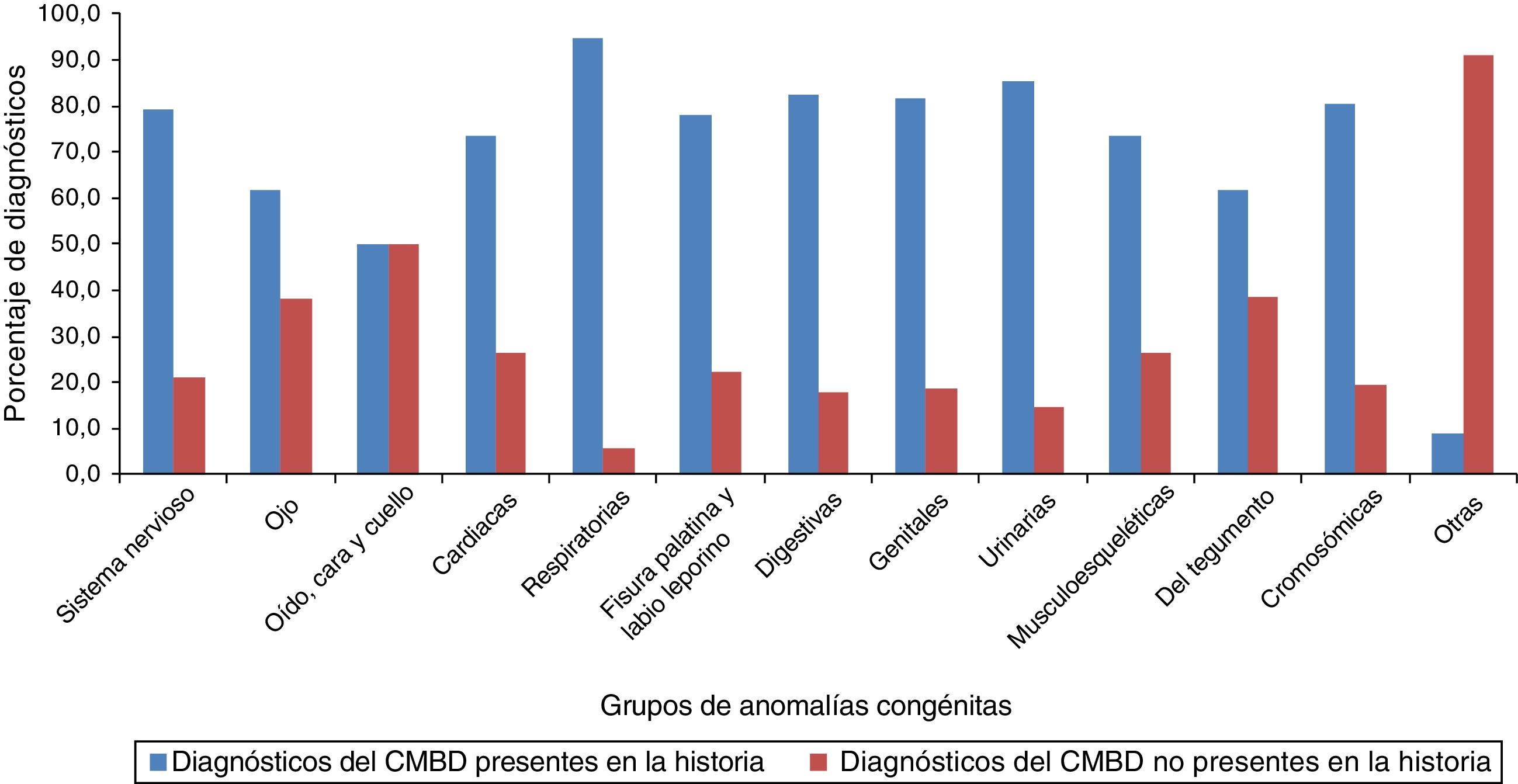
Las frecuencias relativas de los diagnósticos codificados en el CMBD como anomalías congénitas se presentan separadamente para los diagnósticos confirmados y los no confirmados tras la revisión de las historias (fig. 1). Para todos los grupos de anomalías congénitas, excepto los grupos «Otras anomalías congénitas» y «Anomalías congénitas de oído, cara y cuello», la proporción de diagnósticos confirmados fue mayor que la de no confirmados. El grupo de anomalías congénitas con mayor número de diagnósticos confirmados (94,4%) fue el grupo «Anomalías congénitas respiratorias», seguido por «Anomalías congénitas urinarias» (85,3%) y «Anomalías congénitas digestivas» (82,4%).
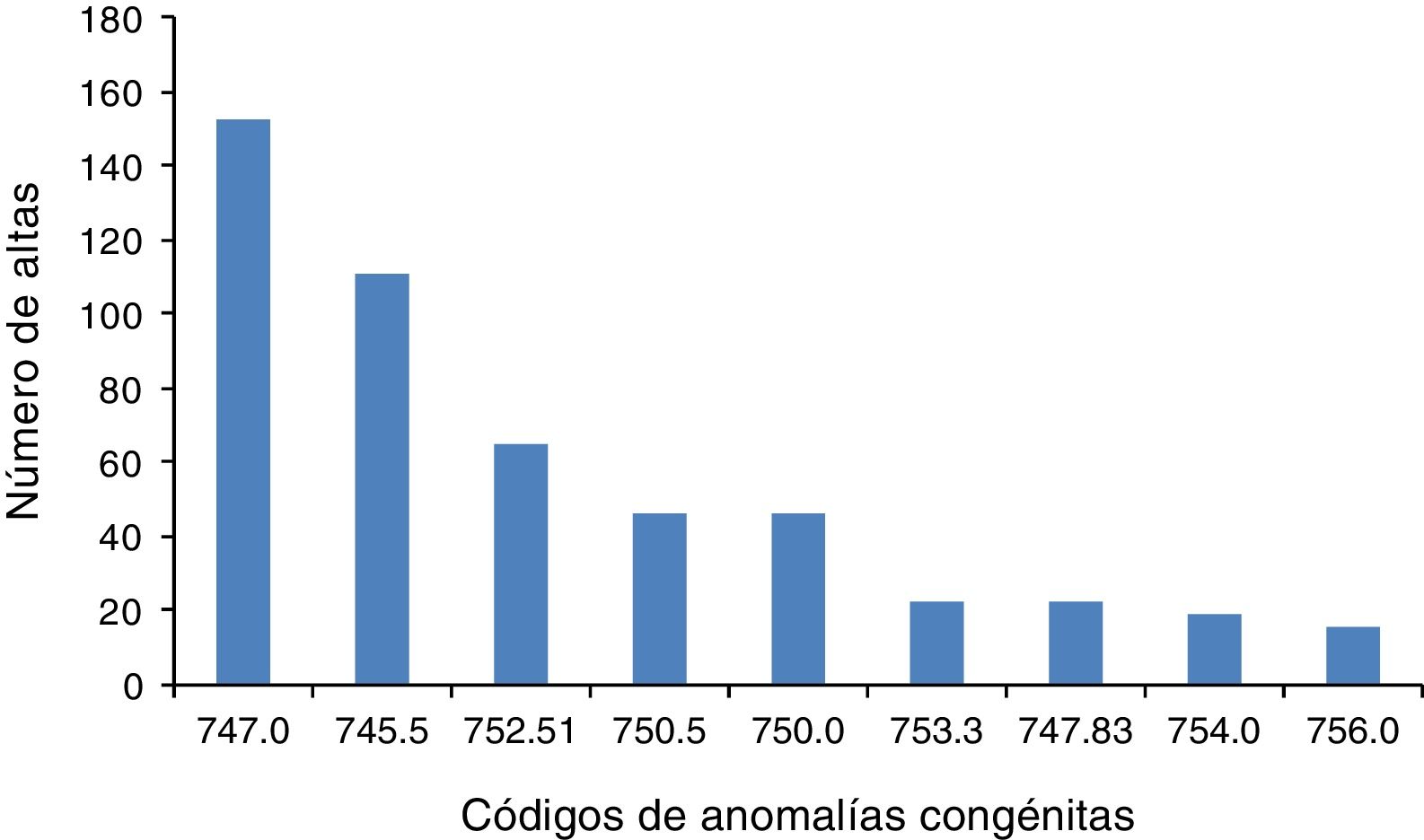
Al considerar los códigos de las anomalías congénitas a 5 dígitos, los diagnósticos más frecuentes obtenidos en los VP se representan en la figura 2. En conjunto suponen el 55,7% de los diagnósticos. Los códigos más frecuentes obtenidos en las altas de los VP fueron el 745.5 (Comunicación interauricular) en el 11,5% de los diagnósticos, el 745.4 (Comunicación interventricular) en el 9,5% y el 747.0 (Ductus arterioso persistente) en el 6,3%.
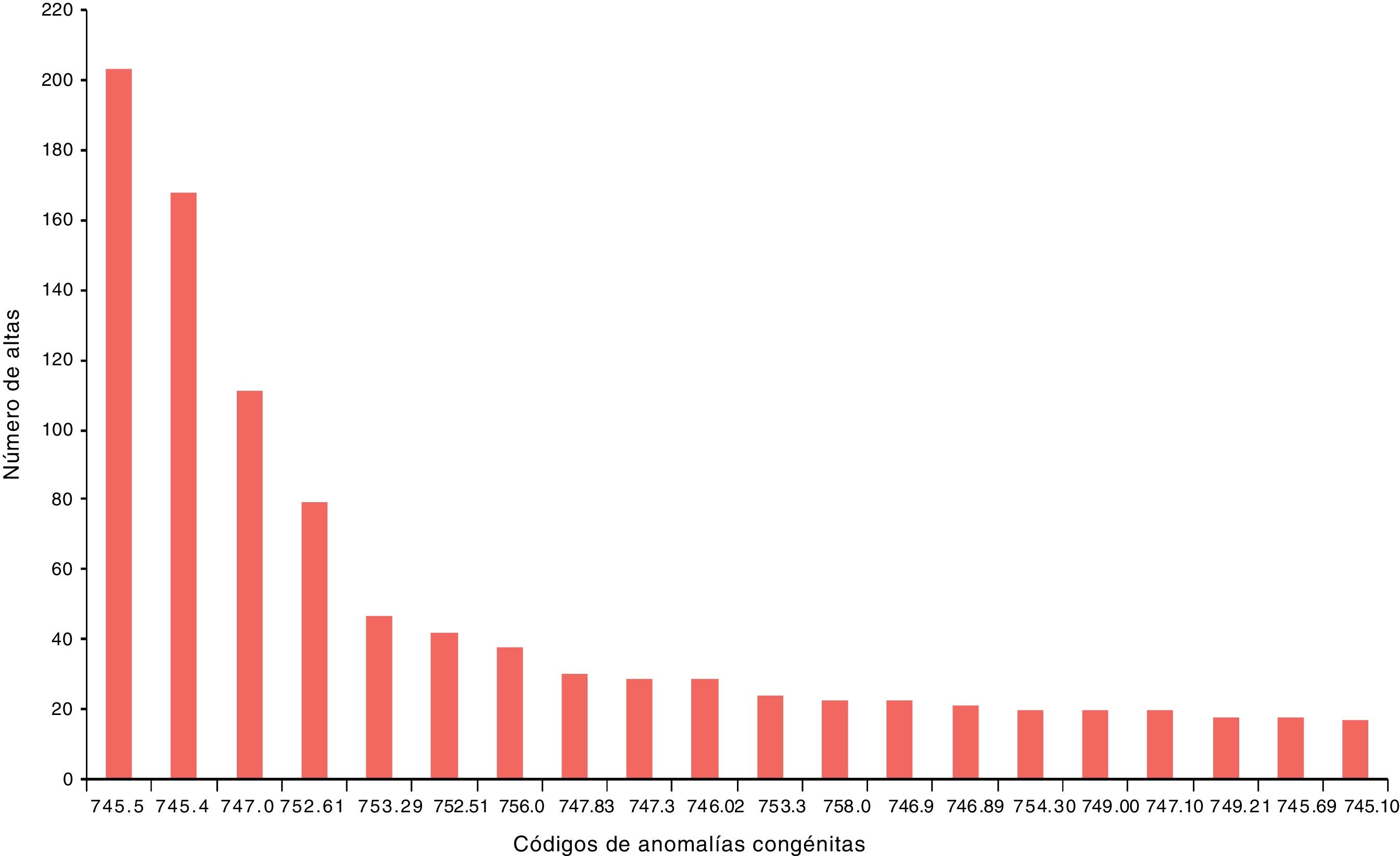
En la figura 3 se presentan los diagnósticos más frecuentes obtenidos para los FP. En conjunto suponen el 61,1% del total de los diagnósticos. En los casos FP, los códigos más frecuentes codificados como anomalías congénitas fueron el 747.0 en el 18,7% de los diagnósticos, el 745.5 en el 13,6% y el 752.51 (criptorquidia) en el 7,9%.
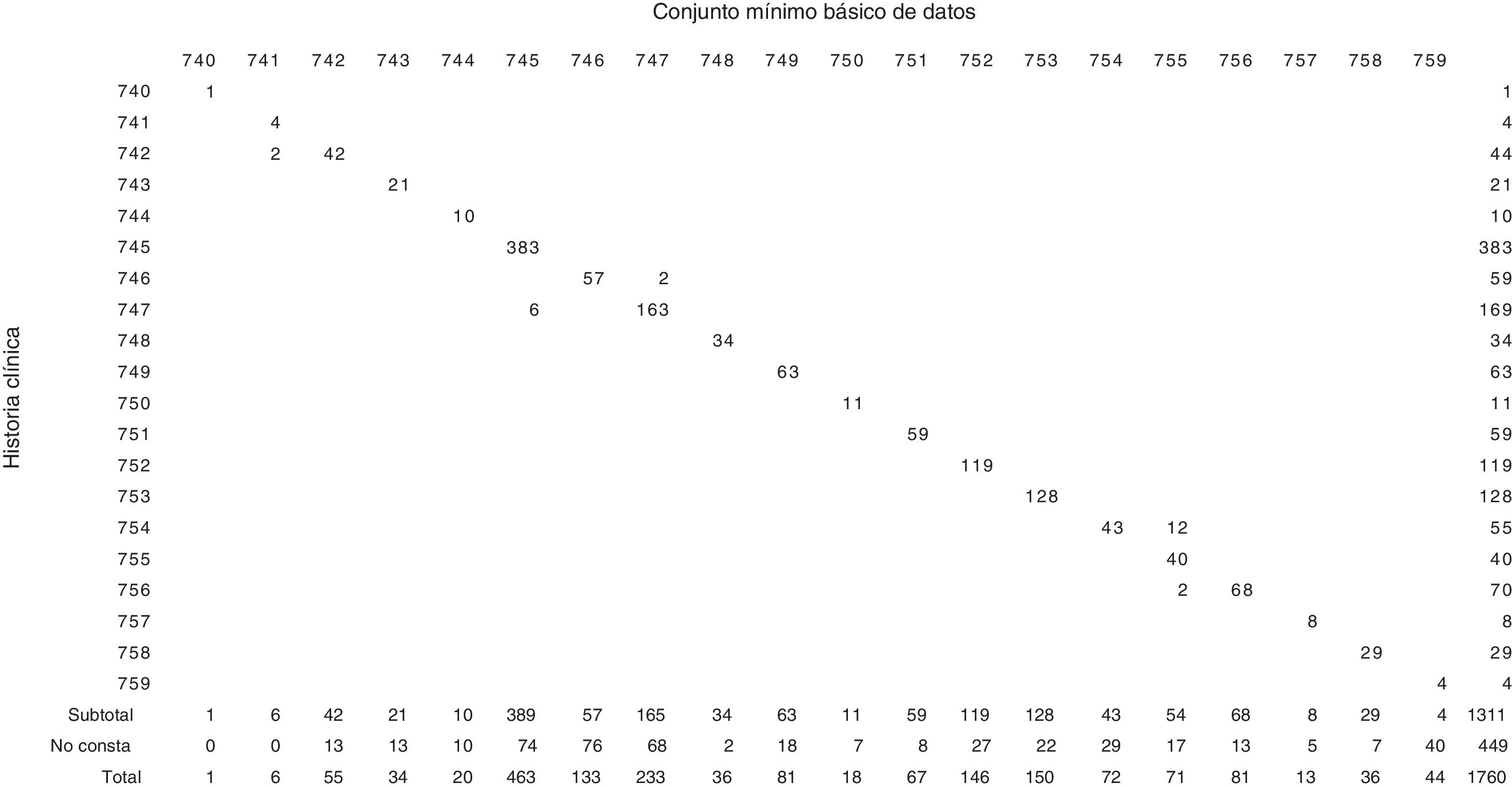
En la figura 4 se presenta la correspondencia entre los códigos a tres dígitos registrados en el CMBD y los códigos obtenidos a partir de las historias. De los 1760 diagnósticos con alguna anomalía congénita codificados en el CMBD, 449 (25,5%) no estaban en la historia. Considerando el total de diagnósticos codificados en el CMBD, se obtuvo una concordancia (kappa) de 0,70 (IC95%: 0,68-0,72). Si consideramos solamente los diagnósticos codificados en el CMBD y registrados en la documentación clínica, el índice fue de 0,98 (IC95%: 0,97-0,99).
Correspondencia entre los códigos utilizados para codificar las anomalías congénitas en el Conjunto Mínimo Básico de Datos y los códigos obtenidos para codificar las anomalías congénitas de las historias clínicas, con la CIE 9-MC.
Códigos de la Clasificación Internacional de Enfermedades 9arevisión-modificación clínica
740: Anencefalia y similar; 741: Espina bífida; 742: Anomalías congénitas del sistema nervioso, otra; 743: Anomalías congénitas del ojo; 744: Anomalías congénitas de oído, cara y cuello; 745: Anomalías congénitas del bulbo arterioso y cierre intracardiaco; 746: Anomalías congénitas del corazón, otra; 747: Anomalías congénitas del aparato circulatorio; 748: Anomalías congénitas del sistema respiratorio; 749: Fisura palatina y labio leporino; 750: Anomalías congénitas del tracto digestivo superior; 751: Anomalías congénitas del aparato digestivo, otra; 752: Anomalías congénitas del aparato urinario; 753: Anomalías congénitas del órgano genital; 754: Anomalías congénitas musculoesqueléticas; 755: Anomalías congénitas del miembro; 756: Anomalías congénitas musculoesqueléticas, otra; 757: Anomalías congénitas del tegumento; 758: Anomalías congénitas cromosómicas; 759: Anomalías congénitas, otra; NC: Diagnóstico del Conjunto Mínimo Básico de Datos no confirmado con la historia clínica.
Igual que en otros registros poblacionales23–25, el CMBD es la principal fuente de información para la identificación de anomalías congénitas mayores en el RPAC-CV. Obtener una proporción de 0,74% de FN confirma que la sistemática de seleccionar los códigos definidos por CIE9-MC como anomalía congénita es adecuada para identificar casos. Además, los cuatro FN fueron identificados en el CMBD de años posteriores durante el seguimiento sistemático que se realiza. Estos datos no coinciden con los obtenidos por Calle y Khoury26, que detectaron un 49% de casos no registrados en las altas hospitalarias.
Por otra parte, la sensibilidad global fue del 68,6%, considerando los casos del RPAC-CV, que incluye a los nacidos vivos, los nacidos muertos y las interrupciones voluntarias del embarazo. Por las características del CMBD no fue posible la detección de anomalías congénitas mayores en interrupciones voluntarias del embarazo ni en nacidos muertos. Así, si para la sensibilidad se utiliza como denominador las anomalías congénitas mayores identificadas en nacidos vivos (1075 casos), su valor asciende al 86,9%. Este resultado es importante para el proceso de recogida de casos en el RPAC-CV, ya que la información clínica hospitalaria es accesible y sin coste.
Si se considera aisladamente la buena concordancia obtenida a tres dígitos entre los códigos de anomalías congénitas de las historias y del CMBD (kappa=0,98), este resultado apuntaría que el CMBD sería una fuente de información adecuada para estimar la prevalencia de anomalías congénitas mayores en menores de un año por grupos de anomalías congénitas. Pero hay que tener en cuenta la proporción de FP obtenida que ascendió al 43,6% de los casos y el hecho de que el 25,5% de los diagnósticos de anomalías congénitas codificados en el CMBD no se confirmaron al revisar las historias. Por tanto, las estimaciones a partir del CMBD de la prevalencia de anomalías congénitas estarían sobrevaloradas.
La sensibilidad global del 68,6% obtenida es superior a la de otros estudios27,28 e inferior a la encontrada por otros autores18,20. El VPP global (56,4%) es muy inferior al obtenido por otros investigadores27,28 y la proporción de los FP (43,6%) es muy superior a la de Callif et al.29 (13,2% y 8,5%). Distintas metodologías podrían explicar estas diferencias, aunque también las diferencias encontradas en VPP entre los hospitales apuntarían hacia diferencias en la validez de las altas de cada centro al incluirse centros de referencia para estas patologías y otros centros que no lo son y, por lo tanto, tienen menos casos de anomalías congénitas mayores.
Se ha encontrado que los casos VP tienen mayor número de altas y diagnósticos de diferentes anomalías congénitas que los FP, lo cual se podría explicar por la mayor gravedad de la patología en los VP, que contribuye a una mayor identificación de casos. La proporción de FP en los que la anomalía congénita se detecta en recién nacidos es superior a la obtenida para los VP, lo cual se podría explicar al detectar una anomalía congénita más grave, porque se enviaría el paciente a hospitales de referencia, donde se produciría el ingreso en días posteriores. La mayor mortalidad hospitalaria entre los VP también apuntaría a una mayor gravedad de anomalías congénitas en estos. Es necesario en estudios posteriores identificar diferencias en códigos de anomalías congénitas para casos VP y FP. Estudios previos30,31 ya indican que el tipo de anomalía congénita está asociado a la identificación y confirmación de casos.
Se encontraron también diferencias entre grupos de anomalías congénitas. La mayor proporción de diagnósticos presentes en ambas fuentes fue para «anomalías congénitas respiratorias», mientras la mayor proporción de diagnósticos no confirmados por historias corresponden a «otras anomalías congénitas», debido a la inclusión de anomalías congénitas inespecíficas que son confirmadas posteriormente.
La mayor proporción de diagnósticos de FP se observó para el conducto arterioso persistente seguido de la comunicación interauricular. Este es un resultado esperado por la definición de caso utilizada (EUROCAT)32. Así, no se considera anomalía congénita mayor el conducto arterioso persistente en menores de 37 semanas de gestación y esta información no siempre está en el CMBD. Además, las comunicaciones interauriculares tipo foramen oval no se consideran anomalías congénitas mayores, pero sí las de tipo ostium secundum, y esta diferenciación no puede realizarse mediante la CIE9-MC.
Una limitación del estudio es la no inclusión de hospitales privados por no estar su CMBD disponible. Sin embargo, la mayor parte de las anomalías congénitas mayores en nacidos en hospitales privados se identificarían a partir del CMBD de hospitales públicos en algún momento. Otra limitación podrían ser los casos incluidos sin información clínica disponible. Sin embargo, dada la baja proporción en que esto ocurrió (2% en casos y 3% en la muestra), es poco probable que sea fuente de sesgo.
La principal limitación del CMBD es el elevado número de FP que proporciona y que hace necesaria la revisión de historias de todos los casos identificados para evitar la sobreestimación de la prevalencia. Tampoco recoge las anomalías congénitas mayores en interrupciones voluntarias del embarazo ni en nacidos muertos, por lo que se necesita incorporar la información del Registro de Interrupciones Voluntarias del Embarazo y de Mortalidad Perinatal para no infraestimar la prevalencia. Por último, la clasificación utilizada en la codificación de los diagnósticos33,34 impide identificar adecuadamente los síndromes35 por la inespecifidad de algunos códigos.
La utilización de múltiples fuentes y la revisión de la documentación clínica son necesarios para mantener la adecuada cobertura y calidad del RPAC-CV30,31. Además, la realización de estudios más detallados que precisen variables asociadas a VP y FP permitirá una extracción de casos del CMBD más eficiente para su utilización en el RPAC-CV.
El Conjunto Mínimo Básico de Datos se utiliza como fuente de información de muchos sistemas de información actuales, pero no se ha estudiado su validez como fuente de identificación de anomalías congénitas, muchas de las cuales no disponen de un código específico en la CIE9.
¿Qué añade el estudio realizado a la literatura?Se ha comprobado la utilidad del Conjunto Mínimo Básico de Datos como fuente de identificación de anomalías congénitas, pero es necesaria la utilización complementaria de otras fuentes y la revisión de la documentación clínica. El disponer de casos validados en el Registro Poblacional de Anomalías Congénitas de la Comunidad Valenciana permite conocer la situación real de estas patologías y desarrollar políticas sanitarias adecuadas para su prevención.
Pere Godoy.
Declaración de transparenciaLa autora principal (garante responsable del manuscrito) afirma que este manuscrito es un reporte honesto, preciso y transparente del estudio que se remite a Gaceta Sanitaria, que no se han omitido aspectos importantes del estudio, y que las discrepancias del estudio según lo previsto (y, si son relevantes, registradas) se han explicado.
Contribuciones de autoríaLos/las autores/as son responsables de la investigación y han participado en su concepto y diseño, análisis e interpretación de los datos, escritura y corrección del manuscrito, y aprueban el texto final que ha sido enviado. C. Cavero y S. Gimeno obtuvieron los datos. C. Martos y M. J. Rabanaque concibieron y diseñaron el estudio, y supervisaron todos los aspectos de su realización. S. Gimeno y O. Zurriaga contribuyeron al análisis de los datos. C. Cavero interpretó los hallazgos y redactó el primer borrador del manuscrito. C. Martos y M.J. Rabanaque realizaron una revisión crítica con importantes contribuciones intelectuales. Todos/as los/las autores/as aportaron ideas e interpretaron los hallazgos y aprobaron la versión final. C. Cavero es la responsable del artículo.
FinanciaciónParcialmente financiado por la Conselleria de Sanitat, Generalitat Valenciana (Proyecto AP-31/11).
Conflictos de interesesNinguno.