La cloración del agua da lugar a la formación de subproductos potencialmente dañinos para la salud, entre elloslos trihalometanos, que se han hallado elevados en algunas zonas de España. En este estudio se investigan los valores de trihalometanos en el agua de consumo suministrada por varios sistemas de abastecimiento de la provincia de Granada, en el área de actuación de la cohorte madres-hijos de la Red INMA (Infancia y Medio Ambiente).
MétodosSe analizaron 82 muestras de agua de consumo en dos campañas de muestreo en invierno y verano de 2006. Se determinó la concentración de cloroformo, bromodiclorometano, dibromoclorometano y bromoformo, siguiendo un procedimiento optimizado basado en cromatografía de gases y espectrometría de masas.
ResultadosEl rango de concentración de trihalometanos totales se situó entre 0,14 y 18,75 μg/l en la campaña de invierno y entre 0,01 y 31,87 μg/l en la de verano. El compuesto mayoritario fue cloroformo. La concentración media de trihalometanos en agua de origen superficial y subterráneo fue de 10,13 y 1,41 μg/l, respectivamente.
ConclusionesLos valores de trihalometanos encontrados son muy inferiores a la concentración máxima admisible (100 μg/l) establecida por la Unión Europea para estos compuestos. Estos valores varían significativamente según el origen del agua, con mayores concentraciones en áreas urbana y semiurbana, donde el agua es mayoritariamente de origen superficial. La presencia de trihalometanos en la zona es menor a la descrita en otras regiones españolas.
Drinking water chlorination generates potentially harmful by-products, such as trihalomethanes. Trihalomethane levels are high in some parts of Spain. The aim of the present study was to investigate trihalomethane concentrations in drinking water from distinct water supplies in the province of Granada, within the framework of the Childhood and Environment (INMA) study.
MethodsEighty-two tap water samples were collected in two campaigns during the winter and summer of 2006. An optimized procedure based on gas chromatography and mass spectrometry was used to determine concentrations of chloroform, bromodichloromethane, dibromochloromethane, and bromoform in the samples.
ResultsTotal trihalomethane concentrations ranged from 0.14 to 18.75 μg/l in winter samples and from 0.01 to 31.87 μg/l in summer samples. The most abundant compound was chloroform. Mean trihalomethane concentrations were 10.13 in surface waters and 1.41 μg/l in ground waters.
ConclusionsThe trihalomethane levels found were considerably below the maximum permitted level of 100 μg/l in the European Union. The values obtained varied widely according to the type of water source: the highest concentrations were found in urban and sub-urban areas, where the water is largely of surface origin. The presence of trihalomethanes was lower than that reported in other Spanish regions.
El cloro añadido como tratamiento de potabilización al agua destinada al consumo puede reaccionar con la materia orgánica presente en el agua, dando lugar a la formación de subproductos de la cloración con propiedades químicas y toxicológicas particulares. Los trihalometanos (THM), junto con los ácidos haloacéticos, son los subproductos más prevalentes en el agua de consumo. Los principales THM son cloroformo, bromodiclorometano (BDCM), dibromoclorometano (DBCM) y bromoformo. La especiación y concentración final de los THM formados depende de varias circunstancias, entre ellas la concentración de materia orgánica e iones bromuro presentes en el agua, el tipo de desinfectante utilizado y la dosis aplicada, el tiempo de residencia en la red de distribución, la temperatura y el pH del agua durante el tratamiento1. Por tanto, cabe esperar variaciones geográficas y estacionales en los valores de THM presentes en el agua potable.
La presencia de THM en el agua de consumo público ha suscitado en los últimos años un creciente interés desde la perspectiva de la salud pública. Desde que fueron detectados por primera vez en el agua a comienzos de la década de los setenta, numerosos estudios epidemiológicos han sugerido la existencia de una posible relación entre la exposición a subproductos de la cloración y efectos perjudiciales sobre la salud humana, como un mayor riesgo de cáncer de vejiga y colorrectal2–6 y problemas respiratorios7,8. Más recientemente también se ha asociado esta exposición con efectos reproductivos adversos, tales como aborto espontáneo, bajo peso al nacer y malformaciones con- génitas9,10.
La preocupación emergente sobre los riesgos para la salud asociados a los THM ha promovido que muchos países industrializados establezcan valores máximos para estos contaminantes en el agua de consumo humano. Así, por ejemplo, una Directiva Europea de 1998 regula los valores máximos aceptables de THM totales y plantea que, a los 5 años de su entrada en vigor, la concentración de THM no debería ser superior a 150 μg/l, y que este límite debe fijarse en 100 μg/l a los 10 años11,12. Asimismo, la Organización Mundial de la Salud ha establecido concentraciones máximas de referencia para las cuatro especies de THM más frecuentes, cloroformo, BDCM, DBCM y bromoformo (300, 60, 100 y 100 μg/l, respectivamente), y aunque no se ha definido para el total de THM se recomienda que los valores de THM en el agua de bebida se mantengan tan bajos como sea posible, siempre y cuando se asegure una desinfección eficaz13.
En 1997, un informe de la Unión Europea señalaba que los valores máximos de THM en Europa se encontraban en Portugal y España14. A pesar del tiempo transcurrido y de que algunos estudios, centrados en su mayoría en poblaciones de la vertiente mediterránea15–17, han descrito THM en agua del grifo, la información concerniente a los valores de estos compuestos en nuestro país es todavía escasa.
La desinfección del agua mediante cloración es adecuada para la eliminación de agentes infecciosos causantes de enfermedades, pero la generación de THM y otros subproductos tóxicos de la cloración supone un riesgo para la salud. A este respecto, el proyecto Infancia y Medio Ambiente (INMA), estudio de cohortes que investiga la influencia de los principales contaminantes del aire, el agua y los alimentos sobre el crecimiento y el desarrollo durante los primeros años de vida18, constituye un escenario particularmente apropiado para evaluar el riesgo de efectos adversos en la salud infantil por exposición a THM. En el marco de este proyecto se pretende describir los valores de subproductos de la clo- ración en el agua de las distintas zonas españolas de estudio, utilizando los THM como marcadores de la mezcla19. La cohorte andaluza de la Red INMA está distribuida en una extensa área de la provincia de Granada, con 50 municipios y más de 500.000 habitantes. El objetivo del presente trabajo es describir la concentración de THM en el agua de consumo suministrada por los principales sistemas que abastecen a los municipios de referencia de la cohorte granadina.
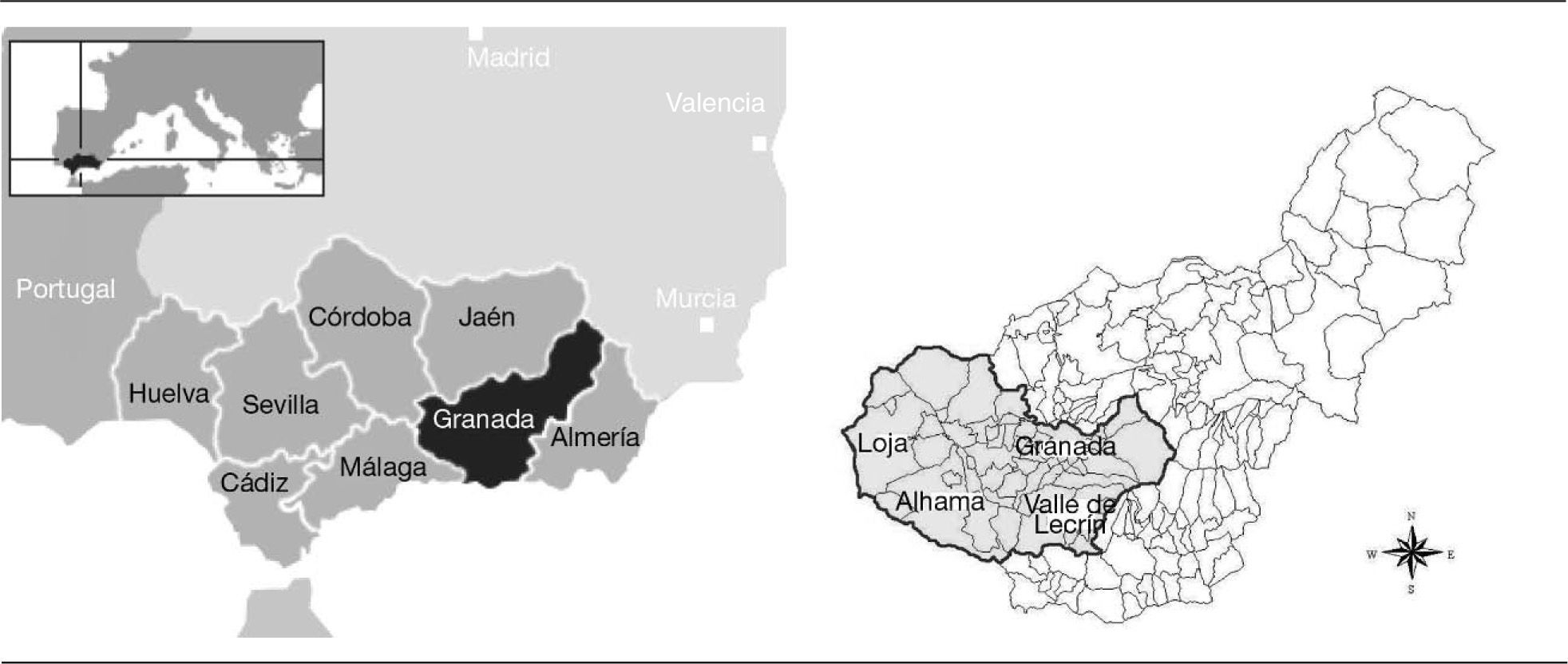
MétodosÁrea de estudioLa cohorte de niños establecida en Granada dentro de la Red INMA está constituida por 700 varones nacidos en el Hospital Universitario San Cecilio entre octubre de 2000 y junio de 2002. La cohorte se distribuye en un área que comprende la zona sur de la capital y 50 municipios de la provincia, lo que supone 40 sistemas de abastecimiento y una población total aproximada de 530.000 habitantes. La zona de estudio coincide con el área de referencia sanitaria del Hospital Universitario San Cecilio de Granada y abarca las comarcas de Granada, Valle de Lecrín, Loja y Alhama (fig. 1), con una extensión superficial aproximada de 3.700 km2. El agua suministrada en la zona procede de varios sistemas principales, los conocidos como Quén- tar-Canales, Vegas del Genil y Los Bermejales, de origen superficial, y Cúllar Vega-Las Gabias, Mancomunidad Río Monachil, Ogíjares y Loja, de origen subterráneo. Éstos abastecen en total a 460.000 habitantes, en su mayoría población urbana, y son gestionados por cuatro empresas diferentes. El resto de abastecimientos corresponde a núcleos semiurbanos y rurales con menos de 10.000 habitantes, donde la gestión del tratamiento y suministro del agua la realizan los ayuntamientos.
Información sobre el origen, el tratamiento y la calidad del agua potableEl Servicio de Sanidad Ambiental de la Consejería de Salud de la Junta de Andalucía proporcionó la información necesaria sobre los distintos sistemas de abastecimiento de la zona y su origen, además de realizar el contacto con las empresas y ayuntamientos implicados en la gestión del agua en el área de estudio. Previamente a la elección de los puntos de muestreo, se envió a las empresas y ayuntamientos una encuesta sobre el origen, el tratamiento y la calidad del agua potable. Estas encuestas fueron diseñadas ad hocdentro de los protocolos establecidos por la Red INMA. En ellas se recoge información básica acerca del tratamiento, el suministro y la calidad del agua potable. El 70% de las encuestas enviadas a ayuntamientos y empresas municipales fueron cumplimentadas y devueltas.
MuestreoEn Granada, donde el clima es mediterráneo continental, la variación de las condiciones climáticas durante el año puede suponer una diferencia importante en la temperatura superficial del agua entre verano e invierno. Por ello, para evaluar la variabilidad estacional de THM se realizaron dos campañas de recogida de agua potable, en invierno (7 y 8 de marzo) y verano (5 y 6 de septiembre) de 2006, midiendo dos veces en cada punto. La selección de los puntos muestreados se realizó teniendo en cuenta los siguientes criterios: a) municipios con mayor número de niños incluidos en la cohorte INMA; b) núcleos del área de estudio con mayor población, y c) principales sistemas de abastecimiento de agua de la zona. De esta forma, se seleccionaron 41 puntos de muestreo distribuidos en 31 municipios, y 25 sistemas de abastecimiento (7 superficiales y 18 subterráneos).
Se recogió agua fría del grifo en locales y en fuentes públicas, dejando correr el agua durante 1 min, evitando la formación de burbujas y cámara de aire entre el agua y el tapón, en 2 viales de vidrio de 40 ml con tapón de rosca y sello de teflón. Los viales contenían 5 mg de tiosulfato sódico para evitar la posterior reacción entre el cloro libre y la materia orgánica residual. Durante la recogida, se determinó la temperatura y el pH de cada muestra. Todas las muestras se mantuvieron a una temperatura de 4 oC durante el almacenamiento y el transporte al laboratorio de análisis. Se siguieron las instrucciones del protocolo establecido por el laboratorio responsable de los análisis para minimizar la pérdida de THM, de manera que las determinaciones analíticas se realizaran siempre antes de transcurridos 14 días tras la recogida, en el Laboratorio de Química Ambiental del Instituto de Investigaciones Químicas y Ambientales (IIQA) del CSIC, en Barcelona.
Análisis experimentalSe analizaron cloroformo, BDCM, DBCM y bromo- formo, siguiendo un procedimiento previamente optimizado20, que consiste en una purga y trampa seguida de una cromatografía de gases acoplada a un espectrómetro de masas. La determinación de los parámetros de temperatura y pH se realizó con un medidor impermeable (Modelo H1 98127-H1 98128, Hanna Instruments, Estados Unidos).
Análisis estadísticoEl análisis estadístico se realizó con el programa SPSS versión 14.0. Debido a que las concentraciones de los compuestos analizados no seguían una distribución normal, se emplearon pruebas no paramétricas para evaluar la variación estacional y de THM según el origen del agua (test de Wilcoxon y prueba de Mann- Whitney, respectivamente), y el test de Spearman para la correlación entre compuestos. El nivel de significación estadística se estableció en un valor de p < 0,05.
ResultadosEn todas las muestras de agua colectadas se detectaron concentraciones cuantificables de, al menos, uno de los THM analizados, y en todos los puntos la concentración fue baja (< 32 pg/l), tanto en invierno como en verano. La concentración media de THM totales fue de 5,64 pg/l (desviación estándar de 6,99 pg/l), alcanzando una concentración máxima de 31,87 pg/l y mínima de 0,01 pg/l, ambas en septiembre. El cloroformo fue el compuesto mayoritario, ya que constituía como promedio un 43% de la concentración de THM totales. Le siguieron BDCM en un 27%, DBCM en un 21% y, por último, bromoformo, representando un 6% del total.
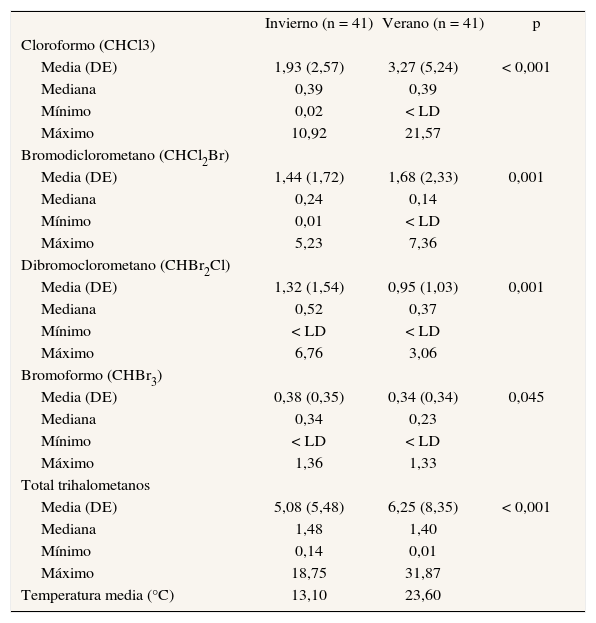
En la tabla 1 se recogen las concentraciones de THM según la campaña de muestreo. La temperatura media del agua recogida en invierno fue de 13,1 oC, y en verano de 23,6 oC. La concentración media de THM totales fue similar en ambos períodos, mientras que la máxima alcanzada en verano casi duplicó a la máxima observada en la campaña de invierno. La presencia de las especies cloradas también fue mayor en septiembre que en marzo. Las concentraciones media y máxima de cloroformo en verano llegaron a doblar a las de invierno. Sin embargo, la concentración de los compuestos bromados disminuyó ligeramente en verano.
Concentración de trihalometanos (μg/l) en las campañas de muestreo
| Invierno (n = 41) | Verano (n = 41) | p | |
| Cloroformo (CHCl3) | |||
| Media (DE) | 1,93 (2,57) | 3,27 (5,24) | < 0,001 |
| Mediana | 0,39 | 0,39 | |
| Mínimo | 0,02 | < LD | |
| Máximo | 10,92 | 21,57 | |
| Bromodiclorometano (CHCl2Br) | |||
| Media (DE) | 1,44 (1,72) | 1,68 (2,33) | 0,001 |
| Mediana | 0,24 | 0,14 | |
| Mínimo | 0,01 | < LD | |
| Máximo | 5,23 | 7,36 | |
| Dibromoclorometano (CHBr2Cl) | |||
| Media (DE) | 1,32 (1,54) | 0,95 (1,03) | 0,001 |
| Mediana | 0,52 | 0,37 | |
| Mínimo | < LD | < LD | |
| Máximo | 6,76 | 3,06 | |
| Bromoformo (CHBr3) | |||
| Media (DE) | 0,38 (0,35) | 0,34 (0,34) | 0,045 |
| Mediana | 0,34 | 0,23 | |
| Mínimo | < LD | < LD | |
| Máximo | 1,36 | 1,33 | |
| Total trihalometanos | |||
| Media (DE) | 5,08 (5,48) | 6,25 (8,35) | < 0,001 |
| Mediana | 1,48 | 1,40 | |
| Mínimo | 0,14 | 0,01 | |
| Máximo | 18,75 | 31,87 | |
| Temperatura media (°C) | 13,10 | 23,60 |
DE: desviación estándar; LD: límite de detección.
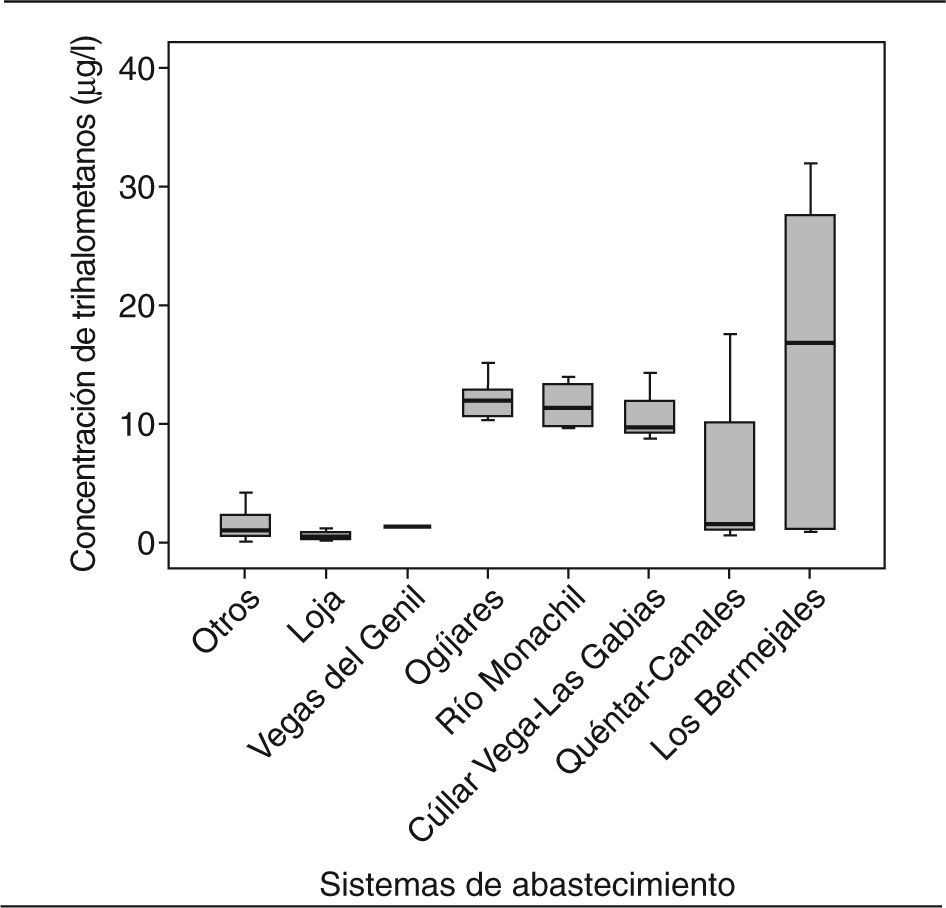
En un 30% de las muestras la concentración de THM superó los 10 pg/l, y en un 58% la concentración estuvo por debajo de 5 pg/l. Los mayores valores se encontraron en municipios abastecidos por el embalse de Los Bermejales (concentración media de 23,25 pg/l), en el sector oeste de la Vega granadina. Le siguen en concentración las muestras recogidas en la ciudad de Granada y en algunos puntos del área metropolitana, procedentes de los sistemas Quéntar-Canales, Cúllar Vega-Las Gabias, Río Monachil y Ogíjares. Las concentraciones más bajas se obtuvieron en el municipio de Loja. En el área rural («Otros») se encontró una concentración media de 2,34 pg/l (fig. 2).
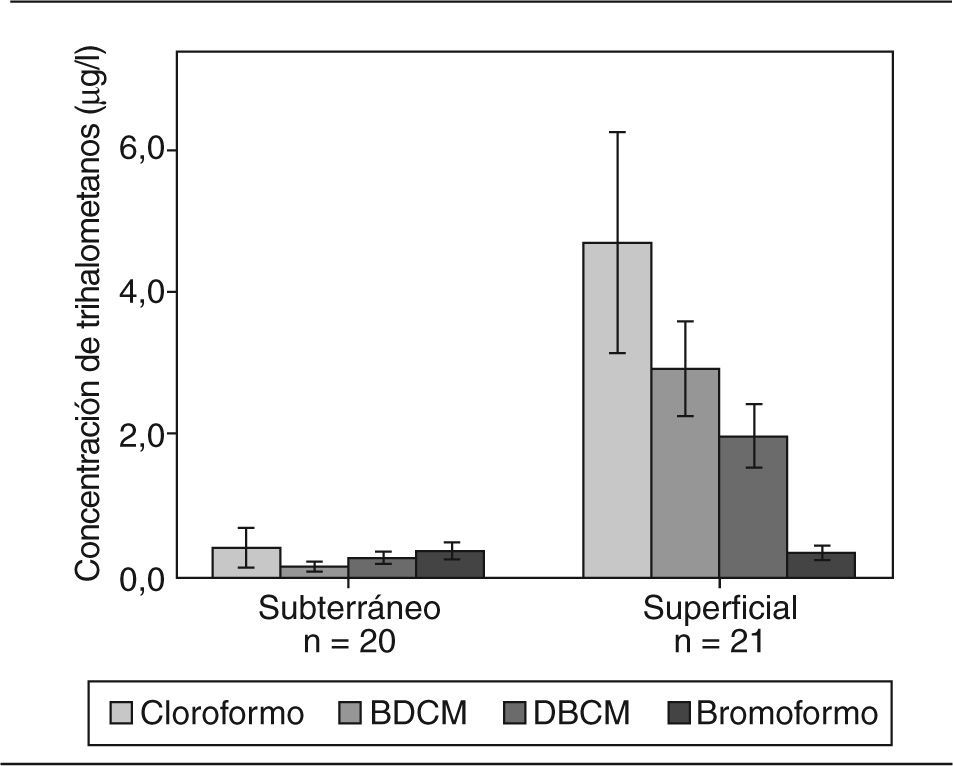
Las muestras de agua de origen subterráneo fueron las que presentaron menores valores de THM. La concentración media de THM en el agua de origen superficial fue de 10,13 pg/l, mientras que en el agua de origen subterráneo fue de 1,41 pg/l (fig. 3). En cuanto a la temperatura del agua, no se encontraron diferencias significativas según el origen. Respecto a los distintos compuestos, encontramos que el cloroformo es el THM que presenta mayor concentración, especialmente en el agua de origen superficial. La concentración de cloroformo fue significativamente superior a la suma de la concentración de las especies bromadas (p < 0,01; coeficiente de Spearman = 0,717). En el agua de origen subterráneo se encontró una mayor proporción de especies bromadas (26% de bromoformo) que en las superficiales.
DiscusiónLa concentración máxima de THM observada en el área de estudio es inferior a la tercera parte del valor máximo admisible de 100 pg/l establecido por la Unión Europea para la suma de estos compuestos. Además, los valores medios encontrados son inferiores a los descritos en otras regiones españolas del norte de la península y de la vertiente mediterránea, como Asturias (concentración media de 22,25 μg/l), Alicante (85,93 μg/l) y Barcelona (63,64 μg/l), referidos por Villanue- va et al16,17 en 1999, y Navarra (44 μg/l)21, así como en otros países europeos22–24. Esto hace pensar que el contenido de THM en los puntos estudiados podría estar directamente relacionado con la calidad del agua antes de su tratamiento, tratándose probablemente de sistemas de abastecimiento con escasa contaminación orgánica. La discrepancia entre nuestros resultados y los publicados en la misma área de estudio por Espigares et al25 en 2003 es aún mayor, aunque las diferencias metodológicas dificultan la comparación.
Es interesante señalar que, independientemente de los valores de THM totales descritos, los resultados obtenidos en este trabajo son similares a los publicados en la mayoría de los estudios que analizan THM en agua de consumo cuando se comparan las distribuciones proporcionales de los distintos compuestos15,23,26,27. El hecho de que predominen las especies cloradas y que la concentración de bromoformo sea muy baja es, según se ha referido en otros estudios, una característica común en las aguas tratadas con cloro y con bajos valores de bromuros en origen26,28, debido posiblemente a que las fuentes que abastecen a la zona estudiada provienen principalmente de sistemas de agua superficial en las que el contenido en bromo es generalmente bajo.
La variación estacional de la concentración de THM fue estadísticamente significativa, aunque menor que la observada en estudios recientemente publicados en Europa (España y Grecia entre ellos) y Estados Unidos, en los que la concentración media de THM en la estación más cálida dobla, al menos, la concentración en la estación fría22,29,30. La diferencia de concentración máxima alcanzada en cada campaña (31,87 frente a 18,75 μg/l) refleja dicha variación estacional, y es coherente con lo publicado en otros estudios de zonas de clima templado, en los que las concentraciones más altas de THM se observaron en verano y otoño, y las más bajas en invierno y primavera27,29,31. En verano, el incremento de temperatura y la disminución del caudal contribuyen a aumentar la concentración de materia orgánica presente en el agua, lo que supone un incremento de los precursores de los THM32. En climas templados, como el de nuestra región, es de esperar que las mayores concentraciones se den en verano.
Las concentraciones más altas de THM se observaron en suministros de agua de origen superficial en la zona de abastecimiento de Los Bermejales, en la que, además, la actividad agrícola podría suponer un mayor aporte de materia orgánica. Igualmente, las mayores concentraciones encontradas en el agua que procede del embalse Quéntar-Canales, principal fuente de abastecimiento de la capital y la comarca de la Vega, sugieren de nuevo que el origen del agua es un factor importante en la formación de THM, coincidiendo con lo publicado por otros autores9,23,33. Así, en la zona rural (municipios de Alhama y Valle de Lecrín, entre otros), donde el 60% de las muestras de agua proceden de sistemas subterráneos, se observaron valores de THM significativamente más bajos que en la zona urbana (concentración media de 2,34 y 9,96 μg/l, respectivamente). El hecho de que el agua de origen subterráneo esté en origen más protegida de las fuentes de contaminación y de los aportes naturales de materia orgánica, se reflejaría en una menor formación de THM29. La mayor presencia de las especies bromadas en el agua subterránea puede explicarse por la mayor concentración de iones de bromo en ella, lo que favorece que durante la cloración del agua se formen ma- yoritariamente bromoformo y DBCM, frente a cloroformo y BDCM en las superficiales31.
Una de las limitaciones principales de este estudio es la falta de datos reglamentarios en algunas áreas, especialmente en los municipios pequeños que cuentan con abastecimientos autónomos, debido a que no todas las encuestas enviadas fueron devueltas, lo que dificulta la evaluación de los resultados obtenidos en estas zonas. Además, no hemos medido parámetros determinantes de la formación de THM, como el contenido en materia orgánica, la turbidez, los iones bromuro, etc., que nos ayudarían a entender mejor la presencia de THM en los distintos abastecimientos.
La selección de los puntos de muestreo se hizo con el propósito de describir los valores ambientales de THM en el agua potable de los municipios de referencia INMA- Granada. A pesar de no haber muestreado en todos ellos, los datos obtenidos pueden considerarse representativos de los principales sistemas que abastecen tanto a la población de la cohorte como a la población de la zona de estudio, ya que el agua analizada procede de 25 sistemas diferentes que abastecen a un 90% de la población del área y a la casi totalidad de municipios de residencia de nuestra cohorte. Un muestreo realizado con mayor frecuencia (p. ej., cada mes), que incluyera puntos de todos los municipios y abastecimientos de la zona, evitaría incertidumbres en cuanto a la posible variabilidad temporal y geográfica de los valores de THM, lo que aumentaría la potencia de un estudio descriptivo como el que se presenta.
Dada la ausencia de trabajos similares relevantes en nuestra región, este estudio permite obtener una aproximación a la presencia de THM en el agua de consumo en el área de Granada. Los valores descritos son inferiores a los encontrados en otras regiones españolas, especialmente en zonas rurales y, en todos los casos, compatibles con las directrices europeas.
AgradecimientosEste trabajo se ha financiado gracias a los proyectos de investigación subvencionados por la Comisión Europea (En- vironmental Reproductive Health-QLK4-1999-01422), el Fondo de Investigaciones Sanitarias (Red de Infancia y Medio Ambiente, INMA-G03/176) y la Consejería de Salud de la Junta de Andalucía (SAS-202/04).
Los autores agradecen la colaboración prestada por Francisco Javier Vílchez y Rafael Acuña, del Servicio de Sanidad Ambiental de la Consejería de Salud de la Junta de Andalucía, para la elaboración de este trabajo. Agradecemos la ayuda técnica de Esther Marco en el laboratorio del CSIC.