Los datos de la Agencia Española de Medicamentos y Productos Sanitarios informan sobre qué comunidades autónomas realizan ensayos clínicos que evalúan medicamentos1. Es difícil conocer el número real de ensayos clínicos que se realizan en España y que evalúan otro tipo de intervenciones. La razón principal es que aquellos que evalúan intervenciones no reguladas (p. ej., cirugía, fisioterapia, psicoterapia) deben ser aprobados por un comité de ética de la investigación2, pero no hay entidad alguna que lleve un registro al respecto. Muchos ensayos clínicos que evalúan este tipo de intervenciones son registrados de manera prospectiva o retrospectiva, pues muchas revistas lo exigen para publicar los resultados3.
En marzo de 2024 se realizó una revisión sistemática de los cuatro registros (European Union Clinical Trials Register [EUCTR], ClinicalTrials.gov, International Standard Randomised Controlled Trial Number [ISRCTN] y Deutsches Register Klinischer Studien [DRKS]) y de la International Clinical Trials Registry Platform (Organización Mundial de la Salud) en cuanto a los ensayos clínicos sobre la COVID-19, cuya metodología ha sido publicada en detalle4. Baste mencionar aquí que el análisis versaba sobre los ensayos clínicos no comerciales, promovidos por investigadores o entidades españolas, y que evaluasen intervenciones de todo tipo. Las estrategias de las búsquedas en los registros mencionados se resumen en el Apéndice, Material suplementario. Se identificaron 170 ensayos clínicos, de los cuales 97 evaluaron medicamentos y 73 intervenciones tales como productos sanitarios, suplementos dietéticos, fisioterapia o plasma de convaleciente4. Entre los ensayos que evaluaron intervenciones no farmacológicas no hay ninguno de intervención comunitaria ni de intervenciones educativas o similares.
Conocer en qué comunidades autónomas radican los promotores de los ensayos clínicos ayuda a conocer, entre otros, el liderazgo investigador de cada territorio. Cataluña y Madrid lideraron el número de ensayos clínicos en este análisis, totalizando 81 ensayos, el 47,6% del total (tabla 1). Cuando el promotor es una institución del Estado (p. ej., el Consejo Superior de Investigaciones Científicas) o una organización profesional (p. ej., la Sociedad Española de Cardiología) que no se puede adscribir a una comunidad autónoma determinada, se incluyó como «No adjudicado»; esto ocurrió en 12 ensayos, el 7,1% del total.
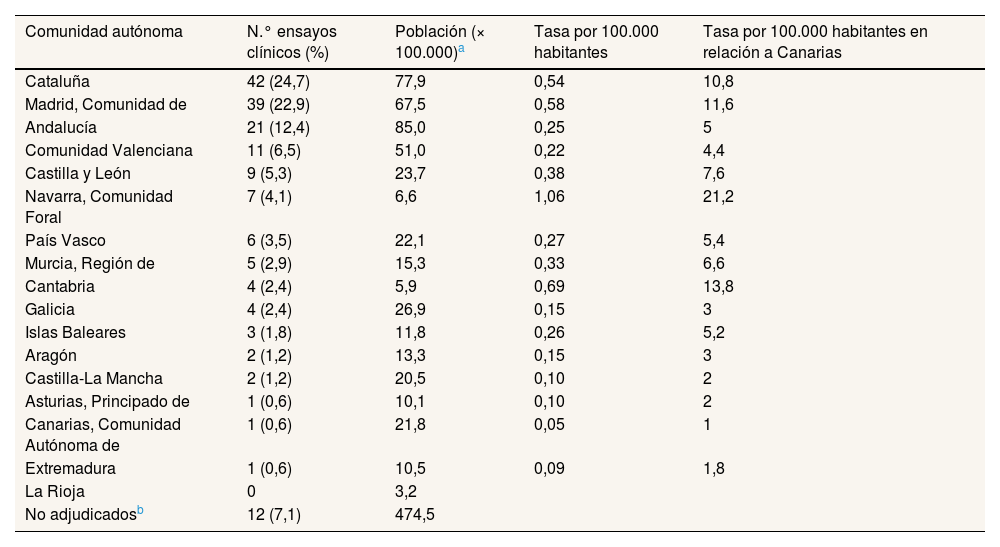
Número de ensayos clínicos según la comunidad autónoma en la que está radicado el promotor y tasa por 100.000 habitantes. Número total de ensayos: 170
| Comunidad autónoma | N.° ensayos clínicos (%) | Población (× 100.000)a | Tasa por 100.000 habitantes | Tasa por 100.000 habitantes en relación a Canarias |
|---|---|---|---|---|
| Cataluña | 42 (24,7) | 77,9 | 0,54 | 10,8 |
| Madrid, Comunidad de | 39 (22,9) | 67,5 | 0,58 | 11,6 |
| Andalucía | 21 (12,4) | 85,0 | 0,25 | 5 |
| Comunidad Valenciana | 11 (6,5) | 51,0 | 0,22 | 4,4 |
| Castilla y León | 9 (5,3) | 23,7 | 0,38 | 7,6 |
| Navarra, Comunidad Foral | 7 (4,1) | 6,6 | 1,06 | 21,2 |
| País Vasco | 6 (3,5) | 22,1 | 0,27 | 5,4 |
| Murcia, Región de | 5 (2,9) | 15,3 | 0,33 | 6,6 |
| Cantabria | 4 (2,4) | 5,9 | 0,69 | 13,8 |
| Galicia | 4 (2,4) | 26,9 | 0,15 | 3 |
| Islas Baleares | 3 (1,8) | 11,8 | 0,26 | 5,2 |
| Aragón | 2 (1,2) | 13,3 | 0,15 | 3 |
| Castilla-La Mancha | 2 (1,2) | 20,5 | 0,10 | 2 |
| Asturias, Principado de | 1 (0,6) | 10,1 | 0,10 | 2 |
| Canarias, Comunidad Autónoma de | 1 (0,6) | 21,8 | 0,05 | 1 |
| Extremadura | 1 (0,6) | 10,5 | 0,09 | 1,8 |
| La Rioja | 0 | 3,2 | ||
| No adjudicadosb | 12 (7,1) | 474,5 |
Para evaluar la capacidad de liderazgo en la investigación de las comunidades autónomas hay que tener en cuenta las diferencias que existen en variables tales como la población, la financiación o el número de investigadores. Como muchos de los ensayos clínicos sobre la COVID-19 no fueron financiados, y estuvieron promovidos por investigadores de distintas disciplinas (médicos, fisioterapeutas, etc.) con actividad pública o privada, de los que conocer un número fiable es prácticamente imposible, la tasa de ensayos clínicos por 100.000 habitantes es útil para poner en perspectiva los datos brutos.
Las comunidades autónomas con las tasas más altas de ensayos clínicos fueron Navarra (1,06) y Cantabria (0,69), y la que tuvo la menor tasa fue Canarias (0,05). La tabla 1 muestra que Navarra y Cantabria realizaron más de 21 y casi 14 veces más ensayos clínicos que Canarias. Por su parte, Murcia (6,6) realizó un 50% más ensayos que la Comunidad Valenciana (4,4).
Este estudio tiene varias limitaciones destacables. Es posible que algún ensayo registrado no haya sido capturado en las búsquedas realizadas. Además, y con mayor importancia, probablemente se realizaron ensayos clínicos con intervenciones no reguladas que no fueron inscritos en los registros, cuyo número es indeterminado. Por otro lado, este estudio no se ocupa de la relevancia ni de la calidad de los ensayos, sino solo de su número. Tampoco tiene en cuenta si los ensayos se iniciaron, realizaron y publicaron4. Finalmente, el hecho de que solo se estudien los ensayos sobre la COVID-19 puede ser un factor de sesgo relevante para la generalización de los resultados obtenidos.
Se deberían hacer estudios con un mayor número de ensayos y sobre todo tipo de patologías para conocer la importancia de las comunidades autónomas como promotoras de ensayos clínicos no comerciales.
Contribuciones de autoríaR. Dal-Ré redactó el borrador. R. Dal-Ré y E. García-Méndez revisaron críticamente el texto e hicieron contribuciones en las sucesivas versiones. Ambas personas firmantes aprobaron la versión final. R. Dal-Ré atestigua que se cumplen los criterios de autoría y que no hay otras personas que los cumplan y que hayan sido excluidas.
FinanciaciónNinguna.
Conflictos de interesesNinguno.