Construir y validar un modelo predictivo del riesgo de consumo de recursos sanitarios elevado, y evaluar su capacidad para identificar pacientes crónicos complejos.
MétodosEstudio transversal realizado en una organización sanitaria integrada sobre datos individuales de residentes 2 años consecutivos (88.795 personas). Variable dependiente: coste sanitario real superior al percentil 95 (P95), incluyendo todos los servicios de la organización sanitaria integrada y las recetas de farmacia. Variables predictoras: edad, sexo, morbilidad (según los clinical risk groups [CRG]) y datos seleccionados de utilización previa (uso de hospitalización, uso de medicación hospitalaria ambulatoria, gasto en recetas de farmacia). Análisis univariado descriptivo. Construcción de un modelo de regresión logística con nivel de confianza del 95%; análisis de validez mediante sensibilidad, especificidad, valor predictivo positivo (VPP) y área bajo la curva ROC (AUC).
ResultadosLas personas con coste >P95 acumulan el 44% del coste sanitario total y se concentran en las categorías ACRG3 (aggregated CRG level 3) de enfermedades crónicas múltiples o graves. La carga de morbilidad aumenta con la edad. En el modelo, todas las variables fueron estadísticamente significativas excepto el sexo. Se obtuvo una sensibilidad del 48,4% (intervalo de confianza [IC]: 46,9%-49,8%), una especificidad del 97,2% (IC: 97,0%-97,3%), un VPP del 46,5% (IC: 45,0%-47,9%) y un AUC de 0,897 (IC: 0,892-0,902).
ConclusionesEl consumo sanitario elevado se relaciona con la morbilidad crónica compleja. Un modelo basado en la edad, la morbilidad y la utilización previa es válido para predecir el riesgo de alto consumo, y así identificar la población diana de estrategias de atención proactiva para pacientes crónicos complejos.
To develop a predictive model for the risk of high consumption of healthcare resources, and assess the ability of the model to identify complex chronic patients.
MethodsA cross-sectional study was performed within a healthcare management organization by using individual data from 2 consecutive years (88,795 people). The dependent variable consisted of healthcare costs above the 95th percentile (P95), including all services provided by the organization and pharmaceutical consumption outside of the institution. The predictive variables were age, sex, morbidity—based on clinical risk groups (CRG)—and selected data from previous utilization (use of hospitalization, use of high-cost drugs in ambulatory care, pharmaceutical expenditure). A univariate descriptive analysis was performed. We constructed a logistic regression model with a 95% confidence level and analyzed sensitivity, specificity, positive predictive values (PPV), and the area under the ROC curve (AUC).
ResultsIndividuals incurring costs >P95 accumulated 44% of total healthcare costs and were concentrated in ACRG3 (aggregated CRG level 3) categories related to multiple chronic diseases. All variables were statistically significant except for sex. The model had a sensitivity of 48.4% (CI: 46.9%-49.8%), specificity of 97.2% (CI: 97.0%-97.3%), PPV of 46.5% (CI: 45.0%-47.9%), and an AUC of 0.897 (CI: 0.892 to 0.902).
ConclusionsHigh consumption of healthcare resources is associated with complex chronic morbidity. A model based on age, morbidity, and prior utilization is able to predict high-cost risk and identify a target population requiring proactive care.
Los modelos de atención sanitaria más avanzados están evolucionando desde una asistencia fragmentada por centros y niveles hacia la integración de servicios, modificando la estrategia asistencial para pasar de una oferta de servicios de respuesta a la demanda a una estrategia proactiva. En este nuevo modelo, las organizaciones sanitarias intentan adelantarse a la demanda identificando necesidades específicas de la población y diversificando adecuadamente la oferta de servicios. Los pacientes crónicos complejos o en situación de fragilidad son los principales beneficiarios de una atención proactiva específica, que asegure una utilización de recursos adecuada y eficiente, y que mejore su calidad y esperanza de vida.
En los últimos años, el abordaje de la cronicidad, entendido en sentido amplio, se ha desarrollado en diferentes direcciones. Entre los instrumentos teóricos de sistematización y evaluación de los modelos de atención a la cronicidad destaca, por su amplia aceptación, el modelo Chronic Care Model1. Desde el Sistema Nacional de Salud, así como desde los diferentes sistemas autonómicos, se han impulsado planes que intentan hacer frente a una realidad epidemiológica marcada por la cronicidad y la longevidad2–6. En estas estrategias aparece repetidamente la necesidad de identificar a los pacientes que han de ser objeto de especial atención.
El abordaje de la estratificación poblacional y de la identificación de pacientes ha utilizado diversas estrategias. Algunas organizaciones han orientado su esfuerzo hacia la predicción del riesgo de reingreso hospitalario, que se considera de alto coste y potencialmente evitable7–10. Otros autores han desarrollado sistemas de ajuste de riesgo basados en diagnósticos y en el coste de años previos para predecir el conjunto de pacientes de alto coste de años venideros11,12. Entre las experiencias más conocidas de utilización práctica de estos modelos destaca la propuesta del Kaiser Permanente, que utiliza una pirámide de estratificación de la población según su perfil de morbilidad crónica y necesidad de recursos13,14.
Cualquiera que sea el enfoque utilizado, la definición de un sistema de identificación de pacientes de alto riesgo implica un conjunto de decisiones previas fundamentales, como por ejemplo la definición misma del riesgo objeto de análisis (reingreso, alto coste…), de sus niveles críticos o del método de identificación. Una de las técnicas más utilizadas y de mayor eficacia, frente a modelos de dintel o basados en criterios de los profesionales asistenciales, es la modelización predictiva mediante modelos de regresión. En general, las variables explicativas más utilizadas en la literatura en estos modelos son de tipo sociodemográfico, de diagnósticos y de utilización previa de recursos asistenciales15.
Serveis de Salut Integrats Baix Empordà (SSIBE) es un proveedor de servicios integrado que dispone de una base de datos con información administrativa, clínica y sobre consumo de recursos de todos los habitantes de la comarca del Baix Empordà, en la provincia de Girona16. Análisis previos sobre la población de SSIBE indican que el coste sanitario es una medida eficaz para caracterizar la complejidad del paciente y el nivel real de utilización de recursos asistenciales; que existe una alta concentración y persistencia de coste sanitario en una pequeña parte de la población, y que el coste sanitario y la carga de morbilidad en la población están fuertemente correlacionados17,18.
Sobre la base del modelo asistencial integrado, en SSIBE se planteó una estrategia de atención a pacientes crónicos complejos con un enfoque proactivo. Para identificar la población diana de esta estrategia se propuso desarrollar un sistema que incorporase la experiencia previa sobre morbilidad y costes, utilizando un parámetro económico como indicador agregado de la utilización de servicios sanitarios.
El objetivo de este trabajo es construir y validar un modelo predictivo del riesgo de consumo de recursos sanitarios elevado, basado en la morbilidad y la utilización previa, y evaluar su capacidad para identificar pacientes crónicos complejos.
MétodosDiseñoEstudio transversal realizado durante los años 2006 y 2007.
ÁmbitoOrganización sanitaria integrada (SSIBE) que incluye cuatro áreas básicas de salud (ABS) semirrurales, el Hospital de Palamós como hospital comarcal del Baix Empordà y el centro sociosanitario Palamós Gent Gran, en la provincia de Girona.
PoblaciónResidentes en las ABS gestionadas por SSIBE en los años 2006 (91.347) y 2007 (93.577), según la base de datos corporativa de SSIBE. El modelo se desarrolló con las personas que estuvieron presentes en ambos años (n=88.795).
VariablesSe obtuvieron datos de 2006 y 2007 de las siguientes variables y fuentes:
- –
Datos demográficos del registro de población de SSIBE: edad y sexo.
- –
Datos de actividad asistencial y consumos sanitarios en todas las unidades asistenciales de SSIBE, obtenidos de su base de datos corporativa.
- –
Morbilidad atendida: obtenida a partir de la codificación mediante la CIE-9-MC de la actividad asistencial del año previo, agrupada según los clinical risk groups (CRG) en su versión 1.6.119,20 siguiendo un procedimiento previamente validado17.
- –
Gasto de recetas de farmacia, según ficheros de facturación facilitados por Catsalut.
- –
Coste sanitario individual, calculado mediante una metodología previamente desarrollada sobre costes reales, que incluye el de todos los servicios prestados por SSIBE y el de las recetas de farmacia dispensadas21,22.
Para el desarrollo del modelo se consideró como variable dependiente el coste sanitario superior al percentil 95 (P95) del coste sanitario total del conjunto de la población en el año 2007 (sí/no). Se escogió como punto de corte el P95 sobre análisis previos de concentración y persistencia del gasto sanitario18, y considerando que el 5% de la población correspondía a un número de personas asequible para realizar estrategias proactivas.
Para la selección de las variables predictoras, anticipando la utilización práctica del modelo, se partió de la premisa de que pudieran estar disponibles al principio de cada año, incluyendo tres grupos de variables:
- a)
Demográficas: sexo y grupo de edad en años (<1, 1-14, 15-24, 25-34, 35-44, 45-54, 55-64, 65-74, 75-84 y ≥85) al iniciar el año 2007.
- b)
Morbilidad: se calculó con la información de diagnósticos y procedimientos del año 2006, utilizando las categorías ACRG3 (aggregated CRG level 3). Se consideró que este nivel, con 44 categorías, aportaba una significación clínica suficiente y discriminaba niveles de gravedad. La categoría 11, Sanos no usuarios, se modificó a la categoría 10, Sanos, si incluía personas con coste sanitario positivo. Así, todos los clasificados como no usuarios tienen coste cero.
- c)
Utilización durante el año 2006: se eligieron por su relación con el coste total elevado, según estudios previos efectuados en el mismo ámbito18, según el coste superior al P95 de la aportación pública de recetas de farmacia del conjunto de la población (sí/no), la medicación hospitalaria de dispensación ambulatoria (MHDA; sí/no) y la hospitalización (sí/no).
Se efectuó un análisis univariado, mediante frecuencias y porcentajes para variables categóricas, y media, mediana y rango intercuartílico (Q1-Q3) para variables cuantitativas. Para la construcción del modelo de regresión logística sólo se incluyeron las personas presentes ambos años del estudio, y se distribuyeron aleatoriamente en dos grupos. El primero incluyó el 70% de la población y se utilizó para estimarlo con un nivel de confianza (IC) del 95%; el 30% restante se utilizó para validarlo. La bondad del ajuste del modelo se evaluó mediante el pseudoestadístico R2 de Nagelkerke (versión ajustada de R2 de Cox y Snell), que determina la proporción de varianza explicada por el modelo en la variable dependiente. El modelo se evaluó mediante la sensibilidad, la especificidad, el valor predictivo positivo (VPP) y el área bajo la curva ROC (AUC) con su IC. Para ello se construyó una tabla 2 ×2 con las variables alto coste real (observado en el año 2007) y predicho según el modelo. Se consideró que el modelo identificaba un individuo como de alto coste si su probabilidad predicha era superior al P95 de la distribución de probabilidad del conjunto de la población23,24. Se utilizó el programa PASW statistics 18.0 (SPSS Inc., an IBM Co. Chigago, Illinois, Estados Unidos).
Aspectos éticosEl proyecto del estudio fue aprobado por el Comité de Investigación Clínica de SSIBE. Dada la metodología del estudio, basado en una revisión retrospectiva de registros clínico-administrativos, no se solicitó consentimiento informado. La extracción de datos fue efectuada por un profesional de SSIBE y su manejo se efectuó de manera anónima.
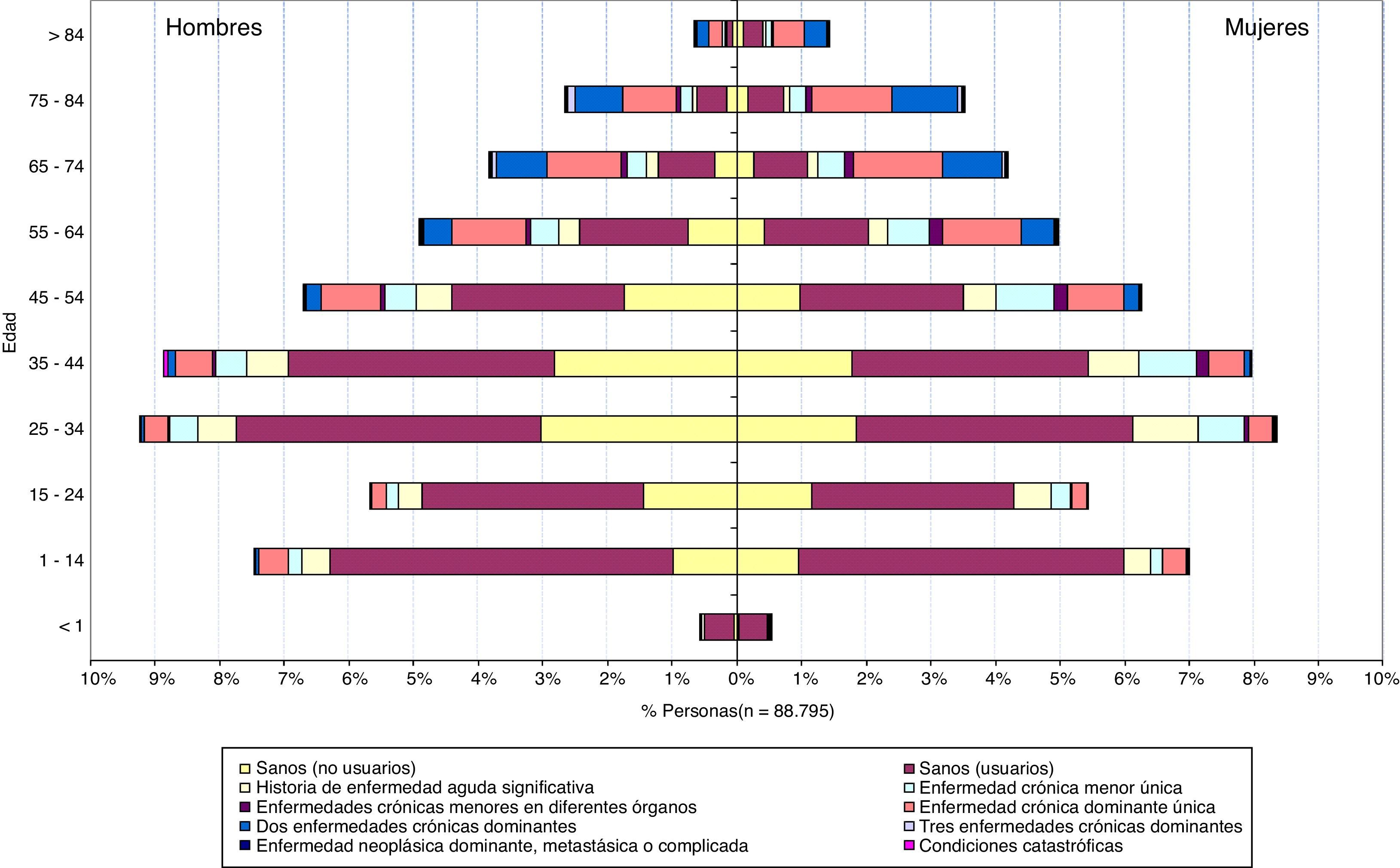
ResultadosLas características sociodemográficas y de morbilidad de la población incluida, presente en los 2 años del estudio (N=88.795), se reflejan en la figura 1. La edad media fue de 39,5 años (desviación estándar [DE]: 24,5 años), y la proporción de mujeres (49,5%) y hombres fue similar. En cada estrato de edad y sexo se incluyó la distribución de morbilidad utilizando los estados de salud de los CRG. Dado que el estado 1-Sanos contiene dos grupos de personas diferenciados, los que contactan con el sistema sanitario y los que no contactan, correspondientes al ACRG3 11-Sanos no usuarios, los pacientes clasificados en este ACRG3 11 se añadieron como un estado de salud más. Este desdoblamiento permite apreciar que aparecen en ambos sexos y en todos los grupos de edad, aunque son más numerosos entre los 15 y los 55 años. Hasta los 55 años de edad, más del 60% de los pacientes en cada grupo se incluyen en el estado de salud Sanos (usuarios y no usuarios). A partir de esta edad la proporción disminuye por debajo del 50%, conforme se incrementa la proporción de pacientes con diferentes combinaciones de enfermedades crónicas de diferente gravedad.
En el cálculo del coste sanitario medio y el del P95 se incluyó toda la población residente cada uno de los años. El coste sanitario total medio fue de 625,8 € (DE: 2283,0 €) en 2006 y de 685,5 € (DE: 2250,9 €) en 2007. El P95 fue 2400,0 € en 2006 y 2673,0 € en 2007. De las 88.795 personas presentes los 2 años, 82.258 (92,6%) tuvieron ambos años del estudio un coste inferior o igual al P95, y 2129 (2,4%) tuvieron un coste superior al P95. El resto de la población (4408 personas, 5%) fueron de alto coste sólo uno de los 2 años del estudio.
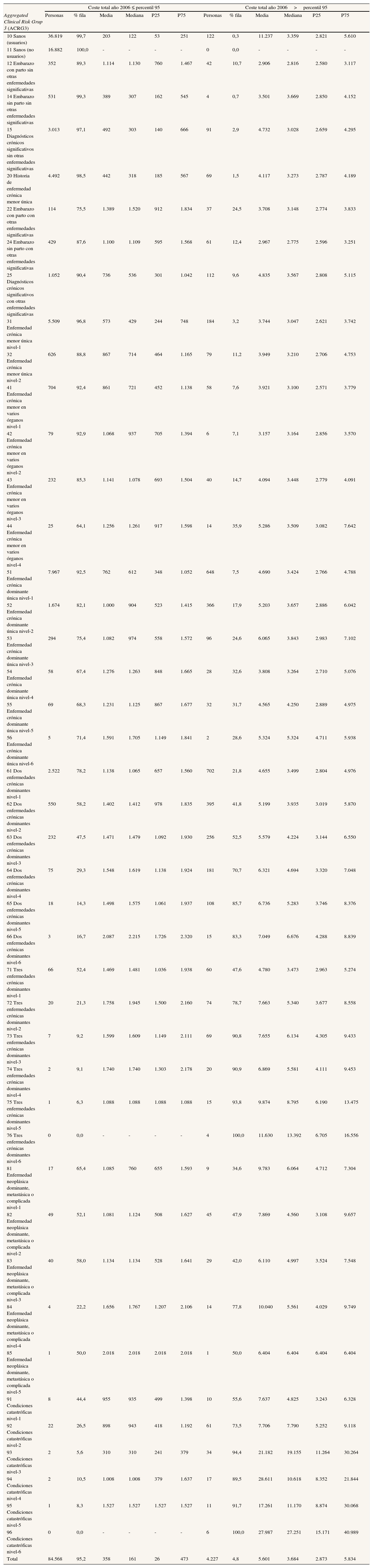
En la tabla 1 se muestra la distribución de la población y el coste sanitario incurrido según morbilidad (estratificada según los ACRG3) para dos subgrupos: el de coste inferior o igual al P95 y el de coste superior al P95, referidos al año 2006. Los datos que se muestran en la tabla se refieren tan sólo a las personas presentes en los 2 años del estudio.
Coste sanitario total en el año 2006 distribuido según morbilidada
| Coste total año 2006 ≤ percentil 95 | Coste total año 2006>percentil 95 | |||||||||||
| Aggregated Clinical Risk Grup 3 (ACRG3) | Personas | % fila | Media | Mediana | P25 | P75 | Personas | % fila | Media | Mediana | P25 | P75 |
| 10 Sanos (usuarios) | 36.819 | 99,7 | 203 | 122 | 53 | 251 | 122 | 0,3 | 11.237 | 3.359 | 2.821 | 5.610 |
| 11 Sanos (no usuarios) | 16.882 | 100,0 | - | - | - | - | 0 | 0,0 | - | - | - | - |
| 12 Embarazo con parto sin otras enfermedades significativas | 352 | 89,3 | 1.114 | 1.130 | 760 | 1.467 | 42 | 10,7 | 2.906 | 2.816 | 2.580 | 3.117 |
| 14 Embarazo sin parto sin otras enfermedades significativas | 531 | 99,3 | 389 | 307 | 162 | 545 | 4 | 0,7 | 3.501 | 3.669 | 2.850 | 4.152 |
| 15 Diagnósticos crónicos significativos sin otras enfermedades significativas | 3.013 | 97,1 | 492 | 303 | 140 | 666 | 91 | 2,9 | 4.732 | 3.028 | 2.659 | 4.295 |
| 20 Historia de enfermedad crónica menor única | 4.492 | 98,5 | 442 | 318 | 185 | 567 | 69 | 1,5 | 4.117 | 3.273 | 2.787 | 4.189 |
| 22 Embarazo con parto con otras enfermedades significativas | 114 | 75,5 | 1.389 | 1.520 | 912 | 1.834 | 37 | 24,5 | 3.708 | 3.148 | 2.774 | 3.833 |
| 24 Embarazo sin parto con otras enfermedades significativas | 429 | 87,6 | 1.100 | 1.109 | 595 | 1.568 | 61 | 12,4 | 2.967 | 2.775 | 2.596 | 3.251 |
| 25 Diagnósticos crónicos significativos con otras enfermedades significativas | 1.052 | 90,4 | 736 | 536 | 301 | 1.042 | 112 | 9,6 | 4.835 | 3.567 | 2.808 | 5.115 |
| 31 Enfermedad crónica menor única nivel-1 | 5.509 | 96,8 | 573 | 429 | 244 | 748 | 184 | 3,2 | 3.744 | 3.047 | 2.621 | 3.742 |
| 32 Enfermedad crónica menor única nivel-2 | 626 | 88,8 | 867 | 714 | 464 | 1.165 | 79 | 11,2 | 3.949 | 3.210 | 2.706 | 4.753 |
| 41 Enfermedad crónica menor en varios órganos nivel-1 | 704 | 92,4 | 861 | 721 | 452 | 1.138 | 58 | 7,6 | 3.921 | 3.100 | 2.571 | 3.779 |
| 42 Enfermedad crónica menor en varios órganos nivel-2 | 79 | 92,9 | 1.068 | 937 | 705 | 1.394 | 6 | 7,1 | 3.157 | 3.164 | 2.856 | 3.570 |
| 43 Enfermedad crónica menor en varios órganos nivel-3 | 232 | 85,3 | 1.141 | 1.078 | 693 | 1.504 | 40 | 14,7 | 4.094 | 3.448 | 2.779 | 4.091 |
| 44 Enfermedad crónica menor en varios órganos nivel-4 | 25 | 64,1 | 1.256 | 1.261 | 917 | 1.598 | 14 | 35,9 | 5.286 | 3.509 | 3.082 | 7.642 |
| 51 Enfermedad crónica dominante única nivel-1 | 7.967 | 92,5 | 762 | 612 | 348 | 1.052 | 648 | 7,5 | 4.690 | 3.424 | 2.766 | 4.788 |
| 52 Enfermedad crónica dominante única nivel-2 | 1.674 | 82,1 | 1.000 | 904 | 523 | 1.415 | 366 | 17,9 | 5.203 | 3.657 | 2.886 | 6.042 |
| 53 Enfermedad crónica dominante única nivel-3 | 294 | 75,4 | 1.082 | 974 | 558 | 1.572 | 96 | 24,6 | 6.065 | 3.843 | 2.983 | 7.102 |
| 54 Enfermedad crónica dominante única nivel-4 | 58 | 67,4 | 1.276 | 1.263 | 848 | 1.665 | 28 | 32,6 | 3.808 | 3.264 | 2.710 | 5.076 |
| 55 Enfermedad crónica dominante única nivel-5 | 69 | 68,3 | 1.231 | 1.125 | 867 | 1.677 | 32 | 31,7 | 4.565 | 4.250 | 2.889 | 4.975 |
| 56 Enfermedad crónica dominante única nivel-6 | 5 | 71,4 | 1.591 | 1.705 | 1.149 | 1.841 | 2 | 28,6 | 5.324 | 5.324 | 4.711 | 5.938 |
| 61 Dos enfermedades crónicas dominantes nivel-1 | 2.522 | 78,2 | 1.138 | 1.065 | 657 | 1.560 | 702 | 21,8 | 4.655 | 3.499 | 2.804 | 4.976 |
| 62 Dos enfermedades crónicas dominantes nivel-2 | 550 | 58,2 | 1.402 | 1.412 | 978 | 1.835 | 395 | 41,8 | 5.199 | 3.935 | 3.019 | 5.870 |
| 63 Dos enfermedades crónicas dominantes nivel-3 | 232 | 47,5 | 1.471 | 1.479 | 1.092 | 1.930 | 256 | 52,5 | 5.579 | 4.224 | 3.144 | 6.550 |
| 64 Dos enfermedades crónicas dominantes nivel-4 | 75 | 29,3 | 1.548 | 1.619 | 1.138 | 1.924 | 181 | 70,7 | 6.321 | 4.694 | 3.320 | 7.048 |
| 65 Dos enfermedades crónicas dominantes nivel-5 | 18 | 14,3 | 1.498 | 1.575 | 1.061 | 1.937 | 108 | 85,7 | 6.736 | 5.283 | 3.746 | 8.376 |
| 66 Dos enfermedades crónicas dominantes nivel-6 | 3 | 16,7 | 2.087 | 2.215 | 1.726 | 2.320 | 15 | 83,3 | 7.049 | 6.676 | 4.288 | 8.839 |
| 71 Tres enfermedades crónicas dominantes nivel-1 | 66 | 52,4 | 1.469 | 1.481 | 1.036 | 1.938 | 60 | 47,6 | 4.780 | 3.473 | 2.963 | 5.274 |
| 72 Tres enfermedades crónicas dominantes nivel-2 | 20 | 21,3 | 1.758 | 1.945 | 1.500 | 2.160 | 74 | 78,7 | 7.663 | 5.340 | 3.677 | 8.558 |
| 73 Tres enfermedades crónicas dominantes nivel-3 | 7 | 9,2 | 1.599 | 1.609 | 1.149 | 2.111 | 69 | 90,8 | 7.655 | 6.134 | 4.305 | 9.433 |
| 74 Tres enfermedades crónicas dominantes nivel-4 | 2 | 9,1 | 1.740 | 1.740 | 1.303 | 2.178 | 20 | 90,9 | 6.869 | 5.581 | 4.111 | 9.453 |
| 75 Tres enfermedades crónicas dominantes nivel-5 | 1 | 6,3 | 1.088 | 1.088 | 1.088 | 1.088 | 15 | 93,8 | 9.874 | 8.795 | 6.190 | 13.475 |
| 76 Tres enfermedades crónicas dominantes nivel-6 | 0 | 0,0 | - | - | - | - | 4 | 100,0 | 11.630 | 13.392 | 6.705 | 16.556 |
| 81 Enfermedad neoplásica dominante, metastásica o complicada nivel-1 | 17 | 65,4 | 1.085 | 760 | 655 | 1.593 | 9 | 34,6 | 9.783 | 6.064 | 4.712 | 7.304 |
| 82 Enfermedad neoplásica dominante, metastásica o complicada nivel-2 | 49 | 52,1 | 1.081 | 1.124 | 508 | 1.627 | 45 | 47,9 | 7.869 | 4.560 | 3.108 | 9.657 |
| 83 Enfermedad neoplásica dominante, metastásica o complicada nivel-3 | 40 | 58,0 | 1.134 | 1.134 | 528 | 1.641 | 29 | 42,0 | 6.110 | 4.997 | 3.524 | 7.548 |
| 84 Enfermedad neoplásica dominante, metastásica o complicada nivel-4 | 4 | 22,2 | 1.656 | 1.767 | 1.207 | 2.106 | 14 | 77,8 | 10.040 | 5.561 | 4.029 | 9.749 |
| 85 Enfermedad neoplásica dominante, metastásica o complicada nivel-5 | 1 | 50,0 | 2.018 | 2.018 | 2.018 | 2.018 | 1 | 50,0 | 6.404 | 6.404 | 6.404 | 6.404 |
| 91 Condiciones catastróficas nivel-1 | 8 | 44,4 | 955 | 935 | 499 | 1.398 | 10 | 55,6 | 7.637 | 4.825 | 3.243 | 6.328 |
| 92 Condiciones catastróficas nivel-2 | 22 | 26,5 | 898 | 943 | 418 | 1.192 | 61 | 73,5 | 7.706 | 7.790 | 5.252 | 9.118 |
| 93 Condiciones catastróficas nivel-3 | 2 | 5,6 | 310 | 310 | 241 | 379 | 34 | 94,4 | 21.182 | 19.155 | 11.264 | 30.264 |
| 94 Condiciones catastróficas nivel-4 | 2 | 10,5 | 1.008 | 1.008 | 379 | 1.637 | 17 | 89,5 | 28.611 | 10.618 | 8.352 | 21.844 |
| 95 Condiciones catastróficas nivel-5 | 1 | 8,3 | 1.527 | 1.527 | 1.527 | 1.527 | 11 | 91,7 | 17.261 | 11.170 | 8.874 | 30.068 |
| 96 Condiciones catastróficas nivel-6 | 0 | 0,0 | - | - | - | - | 6 | 100,0 | 27.987 | 27.251 | 15.171 | 40.989 |
| Total | 84.568 | 95,2 | 358 | 161 | 26 | 473 | 4.227 | 4,8 | 5.601 | 3.684 | 2.873 | 5.834 |
P25: percentil 25; P75: percentil 75.
Se observa que hay pacientes de alto coste en cualquiera de los ACRG3, y que en cada una de las categorías de ACRG3 el coste medio de los pacientes de alto coste es al menos tres veces mayor que el de los pacientes clasificados en el grupo de menor coste. La proporción de casos que son de alto coste dentro de un mismo ACRG3 varía considerablemente, aumentando conforme aumenta la carga de morbilidad. El conjunto de pacientes de alto coste representa el 44% del coste sanitario total.
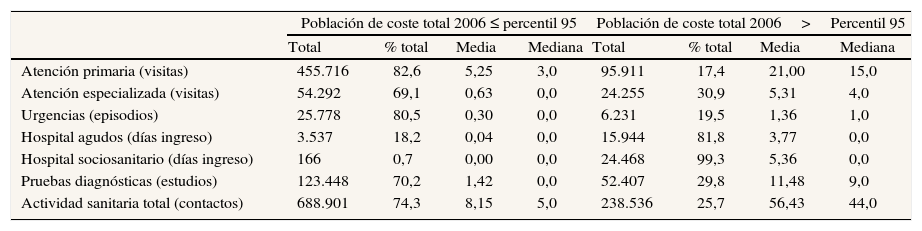
En términos de utilización de servicios sanitarios, la tabla 2 muestra que pertenecer al grupo de alto coste multiplica por cuatro el número de visitas en atención primaria, por nueve el número de visitas en atención especializada, por cinco el número de visitas a urgencias hospitalarias, por 90 el de estancias de hospitalización de agudos, por más de cinco el número de pruebas diagnósticas, y copan la casi totalidad de las estancias en el ámbito sociosanitario.
Utilización de servicios sanitarios. Año 2006a
| Población de coste total 2006 ≤ percentil 95 | Población de coste total 2006>Percentil 95 | |||||||
| Total | % total | Media | Mediana | Total | % total | Media | Mediana | |
| Atención primaria (visitas) | 455.716 | 82,6 | 5,25 | 3,0 | 95.911 | 17,4 | 21,00 | 15,0 |
| Atención especializada (visitas) | 54.292 | 69,1 | 0,63 | 0,0 | 24.255 | 30,9 | 5,31 | 4,0 |
| Urgencias (episodios) | 25.778 | 80,5 | 0,30 | 0,0 | 6.231 | 19,5 | 1,36 | 1,0 |
| Hospital agudos (días ingreso) | 3.537 | 18,2 | 0,04 | 0,0 | 15.944 | 81,8 | 3,77 | 0,0 |
| Hospital sociosanitario (días ingreso) | 166 | 0,7 | 0,00 | 0,0 | 24.468 | 99,3 | 5,36 | 0,0 |
| Pruebas diagnósticas (estudios) | 123.448 | 70,2 | 1,42 | 0,0 | 52.407 | 29,8 | 11,48 | 9,0 |
| Actividad sanitaria total (contactos) | 688.901 | 74,3 | 8,15 | 5,0 | 238.536 | 25,7 | 56,43 | 44,0 |
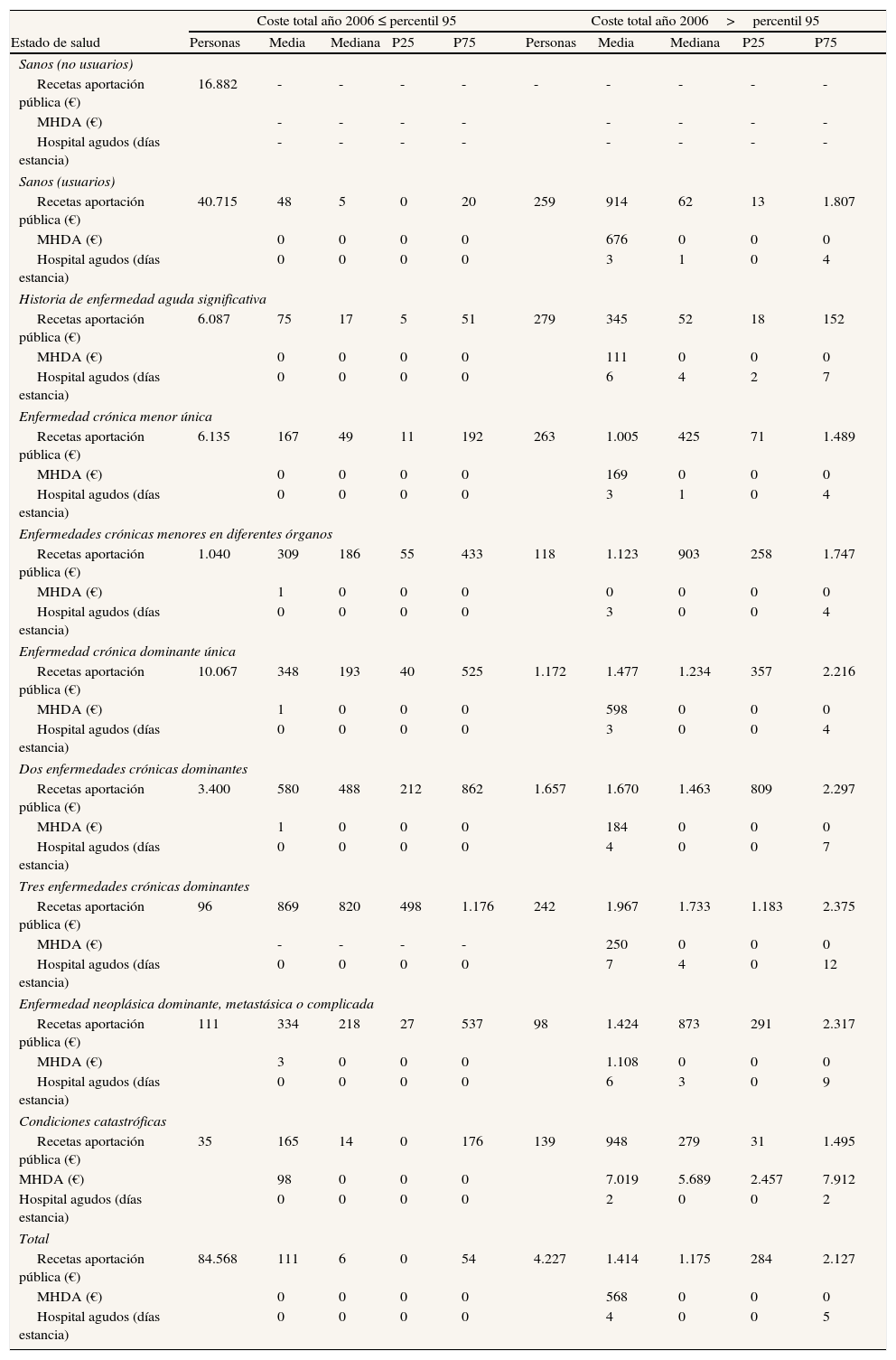
La relación del coste elevado con la morbilidad y el consumo de recursos sanitarios se muestra en la tabla 3, donde se presenta la distribución del consumo de farmacia, tanto de prescripciones ambulatorias (recetas) como de MHDA, y de los días de estancia en hospitalización de agudos, para cada estado de salud de los CRG y comparando los casos de alto coste con el resto. En conjunto, los pacientes del grupo de alto coste acumulan el 39% del coste de recetas de farmacia, el 99% del coste de MHDA y el 82% de las estancias hospitalarias.
Comparación del consumo de farmacia y hospitalización estratificada por estado de salud. Año 2006a
| Coste total año 2006 ≤ percentil 95 | Coste total año 2006>percentil 95 | |||||||||
| Estado de salud | Personas | Media | Mediana | P25 | P75 | Personas | Media | Mediana | P25 | P75 |
| Sanos (no usuarios) | ||||||||||
| Recetas aportación pública (€) | 16.882 | - | - | - | - | - | - | - | - | - |
| MHDA (€) | - | - | - | - | - | - | - | - | ||
| Hospital agudos (días estancia) | - | - | - | - | - | - | - | - | ||
| Sanos (usuarios) | ||||||||||
| Recetas aportación pública (€) | 40.715 | 48 | 5 | 0 | 20 | 259 | 914 | 62 | 13 | 1.807 |
| MHDA (€) | 0 | 0 | 0 | 0 | 676 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 3 | 1 | 0 | 4 | ||
| Historia de enfermedad aguda significativa | ||||||||||
| Recetas aportación pública (€) | 6.087 | 75 | 17 | 5 | 51 | 279 | 345 | 52 | 18 | 152 |
| MHDA (€) | 0 | 0 | 0 | 0 | 111 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 6 | 4 | 2 | 7 | ||
| Enfermedad crónica menor única | ||||||||||
| Recetas aportación pública (€) | 6.135 | 167 | 49 | 11 | 192 | 263 | 1.005 | 425 | 71 | 1.489 |
| MHDA (€) | 0 | 0 | 0 | 0 | 169 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 3 | 1 | 0 | 4 | ||
| Enfermedades crónicas menores en diferentes órganos | ||||||||||
| Recetas aportación pública (€) | 1.040 | 309 | 186 | 55 | 433 | 118 | 1.123 | 903 | 258 | 1.747 |
| MHDA (€) | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 3 | 0 | 0 | 4 | ||
| Enfermedad crónica dominante única | ||||||||||
| Recetas aportación pública (€) | 10.067 | 348 | 193 | 40 | 525 | 1.172 | 1.477 | 1.234 | 357 | 2.216 |
| MHDA (€) | 1 | 0 | 0 | 0 | 598 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 3 | 0 | 0 | 4 | ||
| Dos enfermedades crónicas dominantes | ||||||||||
| Recetas aportación pública (€) | 3.400 | 580 | 488 | 212 | 862 | 1.657 | 1.670 | 1.463 | 809 | 2.297 |
| MHDA (€) | 1 | 0 | 0 | 0 | 184 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 4 | 0 | 0 | 7 | ||
| Tres enfermedades crónicas dominantes | ||||||||||
| Recetas aportación pública (€) | 96 | 869 | 820 | 498 | 1.176 | 242 | 1.967 | 1.733 | 1.183 | 2.375 |
| MHDA (€) | - | - | - | - | 250 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 7 | 4 | 0 | 12 | ||
| Enfermedad neoplásica dominante, metastásica o complicada | ||||||||||
| Recetas aportación pública (€) | 111 | 334 | 218 | 27 | 537 | 98 | 1.424 | 873 | 291 | 2.317 |
| MHDA (€) | 3 | 0 | 0 | 0 | 1.108 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 6 | 3 | 0 | 9 | ||
| Condiciones catastróficas | ||||||||||
| Recetas aportación pública (€) | 35 | 165 | 14 | 0 | 176 | 139 | 948 | 279 | 31 | 1.495 |
| MHDA (€) | 98 | 0 | 0 | 0 | 7.019 | 5.689 | 2.457 | 7.912 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 2 | 0 | 0 | 2 | ||
| Total | ||||||||||
| Recetas aportación pública (€) | 84.568 | 111 | 6 | 0 | 54 | 4.227 | 1.414 | 1.175 | 284 | 2.127 |
| MHDA (€) | 0 | 0 | 0 | 0 | 568 | 0 | 0 | 0 | ||
| Hospital agudos (días estancia) | 0 | 0 | 0 | 0 | 4 | 0 | 0 | 5 | ||
MHDA: medicación hospitalaria de dispensación ambulatoria; P25: percentil 25; P75: percentil 75.
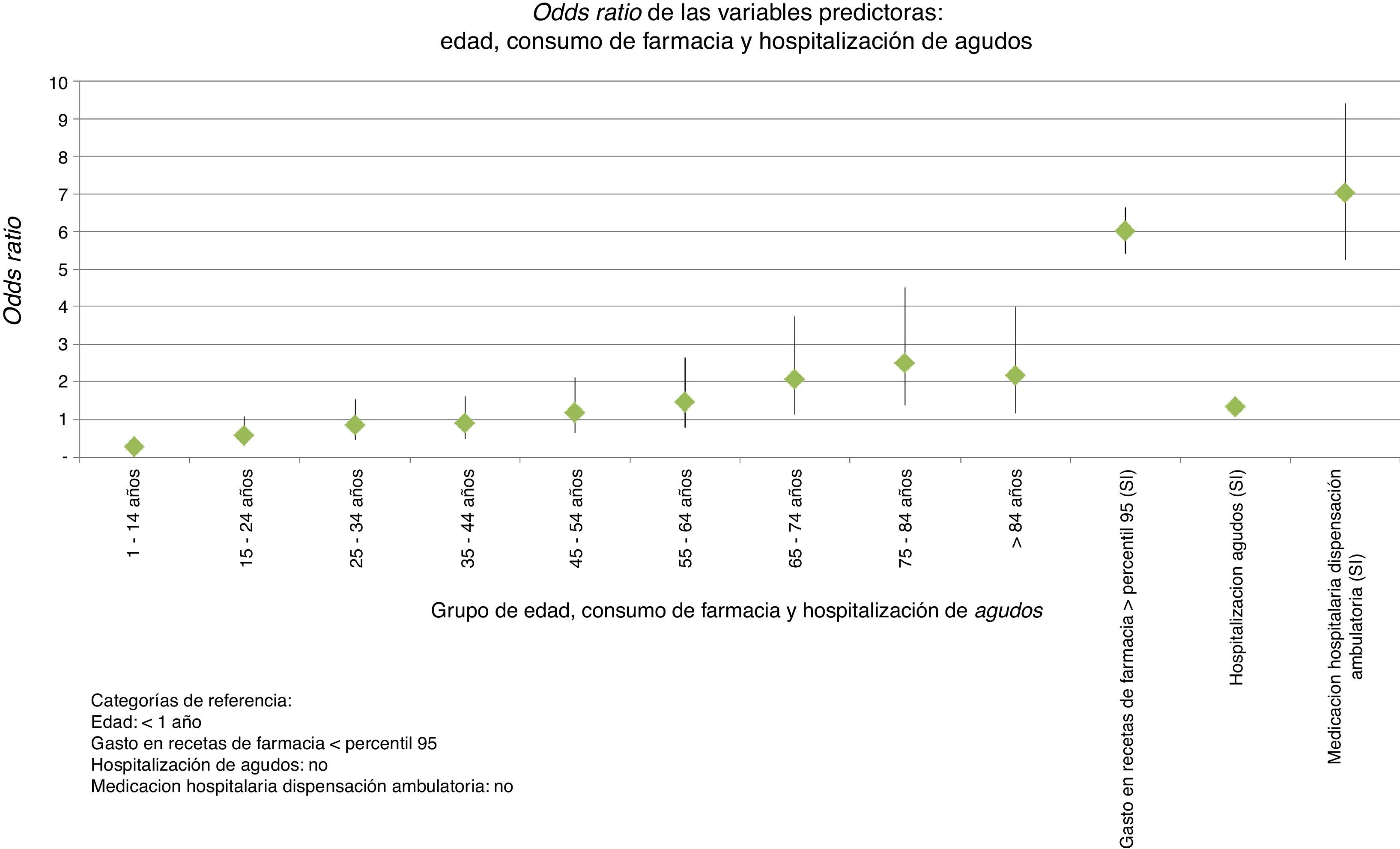
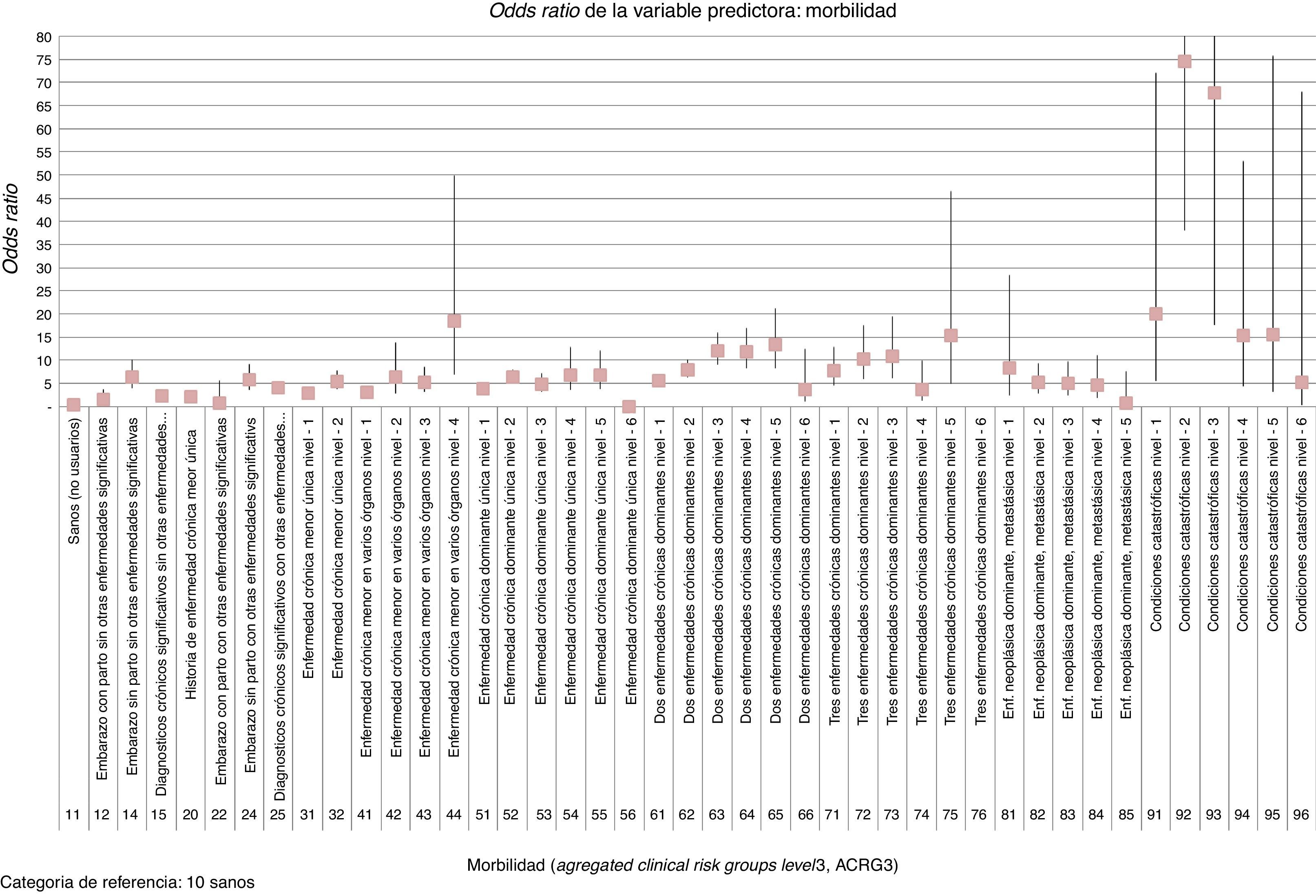
El cálculo del modelo determinó que las variables edad, ACRG3, gasto de recetas de farmacia superior al percentil 95, consumo de MHDA y hospitalización eran estadísticamente significativas como variables predictoras, pero no así el sexo. La varianza explicada por el modelo final utilizado fue del 38,2% (R2 de Nagelkerke=0,382). En la tabla I del Apéndice en la versión online de este artículo se aportan los detalles del modelo desarrollado. Las figuras 2 y 3 muestran las odds-ratio de cada una de las categorías de las variables introducidas finalmente en el modelo.
Para evaluar la capacidad de identificación de las personas clasificadas en el grupo de alto coste se realizó un análisis de la capacidad discriminante del modelo elegido. La sensibilidad fue del 48,4% (IC: 46,9%-49,8%), la especificidad fue del 97,2% (IC: 97,0%-97,3%) y el valor predictivo positivo fue del 46,5% (IC: 45,0%-47,9%). El área bajo la curva ROC fue de 0,897 (IC: 0,892-0,902).
DiscusiónLos resultados de este estudio muestran que, mediante técnicas de modelización aplicadas a una población definida, puede predecirse de manera suficientemente válida el riesgo individual de efectuar un consumo sanitario elevado, considerando las características sociodemográficas, de morbilidad y de utilización previa de recursos como factores predictivos.
Orueta et al.25 incluyen toda la población del País Vasco y utilizan tres sistemas de ajuste de riesgo diferentes, uno de ellos los CRG, para evaluar su capacidad explicativa del gasto sanitario e identificar los pacientes de más alto coste (5% de la población). Nuestro estudio incorpora datos de una mayor amplitud de servicios sanitarios (estimamos que se incluye el 82% del coste total, frente al 72%), y además está basado en una metodología de coste real frente a una de utilización de tarifas, aunque en una población sensiblemente inferior. A pesar de estas diferencias, los valores del AUC para la identificación de los casos de alto coste en ambos estudios para los CRG son similares (0,897 en nuestro estudio y 0,848 en el vasco). Haas et al.26 utilizan seis sistemas de ajuste de riesgo, aunque no los CRG, como medida de la morbilidad para predecir diferentes resultados (hospitalizaciones y reingresos a 30 días, visitas a urgencias, coste total) en una población de tamaño similar a la de nuestro estudio, y no se encuentran diferencias entre ellos. En su caso identifican el 10% de la población de más alto coste con AUC alrededor de 0,75, pero no utilizan los datos de consumo previo como predictores, lo que justifica que nuestros resultados sean ligeramente mejores. Meenan et al.27 muestran valores similares de sensibilidad a los obtenidos por nosotros para cinco modelos de ajuste de riesgo, incluyendo 1,5 millones de personas y centrándose en el 1% de la población de mayor coste. Otros autores28,29 obtienen resultados similares con ligeras variaciones metodológicas. En todos estos trabajos se consideran otras variables (no utilizadas en nuestro estudio), tales como el índice de deprivación MEDEA o el estado de salud autopercibida, como variables predictoras que en general aportan poco valor explicativo a los modelos utilizados.
La aproximación que se ha empleado en este estudio es diferente a la de Billing et al.13 y López-Aguilá et al.15, ya que en estos casos el interés del modelo estaba centrado en la identificación de pacientes con alto riesgo de reingreso hospitalario.
El modelo desarrollado cumple tres condiciones relevantes para facilitar su aplicación práctica. Por una parte, utiliza un nivel de agrupación con suficiente significación clínica para que sea útil y comprensible a los profesionales asistenciales. El segundo aspecto a considerar es que el tamaño de la población seleccionada, fijado en un 5% del total, sería el máximo asumible por los equipos sanitarios para un abordaje proactivo. Finalmente, las variables predictoras utilizadas pueden estar disponibles con un retraso mínimo para su uso. Puede considerase razonable que durante el primer mes del año estén disponibles tanto el cálculo de la morbilidad como los datos de hospitalización y farmacia del año previo, para actualizar el modelo y aplicarlo en el año en curso. Por otro lado, su utilidad radica en la identificación de pacientes con elevadas necesidades de cuidados, donde se supone que la atención proactiva puede mejorar la eficiencia de los cuidados y la calidad de vida de estos pacientes30.
Como limitación, debe tenerse en cuenta que los costes asociados con cada paciente responden a la realidad de la organización donde se ha desarrollado el estudio (validez interna). Además, al introducir el consumo de productos farmacéuticos como elemento predictivo se incorpora el estilo de práctica prescriptora de los profesionales de SSIBE, que puede ser distinto en otra organización18. Por ello, cualquier posible extrapolación a otros ámbitos debe hacerse con mucha precaución, y requeriría una validación y una calibración con datos propios (validez externa).
Otra limitación reseñable es que no se han incluido variables socioeconómicas por falta de disponibilidad sistemática individual. Sin embargo, otros autores que las utilizan señalan su poca aportación a la capacidad predictiva de los modelos utilizados25.
La sensibilidad y el valor predictivo positivo obtenidos son los habituales en este tipo de análisis, y se consideran suficientes para la finalidad que se persigue. En definitiva, un modelo predictivo de riesgo debería tener una aplicación práctica prudente, similar a la que pueda tener un instrumento de cribado: permite detectar las personas con más alta probabilidad de efectuar una elevada utilización de recursos, pero no la asegura. Antes de aplicar una intervención sanitaria determinada, es preciso evaluar de manera individual cada uno de los casos identificados, sea mediante consulta de registros clínicos o presencialmente.
Aunque la variable dependiente del modelo desarrollado tenga una dimensión económica, su utilidad va más allá de la gestión financiera. El riesgo de consumo sanitario total elevado se relaciona con la presencia de condiciones clínicas crónicas y su nivel de complejidad. Por ello, los individuos clasificados como de alto riesgo corresponden a personas con enfermedades crónicas complejas, tributarias de un abordaje asistencial de gestión de casos. En definitiva, un modelo basado en la edad, la morbilidad y la utilización previa permite identificar la población diana de una estrategia de atención proactiva a pacientes crónicos complejos.
El modelo predictivo es un proceso estadístico mediante el cual, a partir del análisis de datos previos, se determinan probabilidades de un acontecimiento futuro. Así, por ejemplo, una estimación de los pacientes con un gasto superior al percentil 95 permite establecer estrategias proactivas de gestión clínica de casos y enfermedades.
¿Qué añade el estudio realizado a la literatura?El modelo predictivo de gasto sanitario individual en una organización sanitaria integrada permite adoptar estrategias de mejora en la gestión clínica de los pacientes a partir de la identificación del riesgo previsto. Las principales barreras para generalizar los modelos predictivos en el sistema de salud son las bases de datos necesarias y la inercia organizativa; sería más fácil si éstas se estandarizaran y los gobiernos las promovieran.
Clara Bermúdez-Tamayo.
Contribuciones de autoríaTodos los autores participaron en el diseño y el desarrollo del estudio previo, así como en la revisión del manuscrito, del cual aprueban su versión final. J. Coderch dirigió el estudio previo y ha coordinado la elaboración del manuscrito y su corrección final. I. Sánchez realizó las técnicas estadísticas para la construcción y la validación del modelo predictivo. P. Ibern ha supervisado todo el proceso, aportando específicamente la visión de experiencias internacionales. M. Carreras efectuó el análisis de costes sanitarios individual. X. Pérez-Berruezo ha desarrollado los aspectos relacionados con la aplicabilidad en los procesos asistenciales. J.M. Inoriza realizó el análisis de actividad y morbilidad, elaboró el informe sobre el estudio previo y efectuó la revisión bibliográfica.
FinanciaciónArtículo elaborado en el marco del proyecto PI12/01355, Efectividad e impacto económico de un programa de atención proactiva a pacientes crónicos complejos identificados mediante un modelo predictivo basado en la morbilidad (ATENPRO), financiado por el Instituto de Salud Carlos III, en la convocatoria 2012 de ayudas del Subprograma de Proyectos de Investigación en Salud, cofinanciado por el Fondo Europeo de Desarrollo Regional (FEDER) de la Unión Europea.
Conflictos de interesesNinguno.
Al Departament de Salut de la Generalitat de Catalunya, que financió el estudio previo Identificació i predicció del risc segons la morbiditat atesa al Baix Empordà18. A Elena Calvo y Maria Lluïsa de La Puente por su confianza e impulso a dicho proyecto. Para la obtención y el tratamiento de la información ha sido imprescindible la colaboración de diversos profesionales de Serveis de Salut Integrats Baix Empordà (SSIBE), en particular de Josep Vilà, Martí Pàmies i Josep Maria Lisbona. A Montse Rovira por su trabajo de edción final del manuscrito.