Se propone una ruta práctica, orientativa y no lineal, para que los equipos de enfermería del Sistema Nacional de Salud transformen las necesidades clínicas en productos sanitarios transferibles, integrando los principios de investigación e innovación responsables (anticipación, reflexividad, inclusión y capacidad de respuesta) y los requisitos del Reglamento (UE) 2017/745 y las normas asociadas (gestión del riesgo y usabilidad). La ruta articula la definición del uso real, la revisión de la evidencia y el paisaje tecnológico, el prototipado y la cocreación, el encaje regulatorio, la estrategia de protección y transferencia, y la evaluación proporcional (usabilidad formativa/sumativa y evidencia clínica). Como demostrador se presenta ERGOMIC, un dispositivo no invasivo para la micción en mujeres en decúbito supino, que aborda una brecha de diseño con dimensión de equidad de género, plan de usabilidad y análisis de ciclo de vida. Esta aproximación facilita soluciones seguras, aceptables y adoptables.
A practical, guiding and non-linear pathway is proposed to help nursing teams within Spain's National Health System transform clinical needs into transferable medical devices, integrating responsible research and innovation principles (anticipation, reflexivity, inclusion and responsiveness) and the requirements of Regulation (EU) 2017/745 and related standards (risk management and usability). The pathway brings together definition of real-world use, review of evidence and the technology landscape, prototyping and co-creation, regulatory alignment, an intellectual property protection and transfer strategy, and proportionate evaluation (formative/summative usability and clinical evidence). As a demonstrator, ERGOMIC —a non-invasive voiding device for women in the supine position— is presented, addressing a design gap with a gender equity dimension, a usability plan and a life cycle assessment. This approach supports solutions that are safe, acceptable and adoptable.
La innovación en tecnología sanitaria y desarrollo de productos sanitarios es una extensión natural de la práctica enfermera cuando se detectan necesidades no resueltas en el punto de atención. En el Sistema Nacional de Salud (SNS), muchas soluciones nacen como adaptaciones informales orientadas a mejorar el confort, la seguridad y la eficiencia del trabajo, pero con menor frecuencia avanzan por circuitos estructurados de innovación y transferencia. Las barreras son conocidas: baja madurez inicial de las ideas, falta de tiempos y de roles definidos, y conocimiento limitado de la propiedad industrial y de los requisitos regulatorios. La experiencia internacional en entornos de apoyo al diseño muestra que la contribución enfermera al diseño y la implementación es iterativa y colaborativa1. Cuando el talento individual se sostiene con mentoría, formación y tiempos protegidos —incluso sin depender necesariamente de financiación competitiva en fases tempranas—, esa capacidad se traduce en proyectos más robustos y transferibles2. Conviene distinguir entre la participación enfermera en proyectos impulsados por terceros y la innovación liderada por enfermería, en la que la necesidad clínica, los criterios de uso y los valores del cuidado guían el diseño y la evaluación. Finalmente, integrar desde el inicio principios de innovación responsable y criterios de usabilidad es un imperativo ético, y además reduce costes y retrasos. Esto es en especial relevante cuando existen inequidades de diseño vinculadas al sesgo sexo-género, frecuentes en las tecnologías históricamente desarrolladas en torno a un «usuario estándar» masculino.
Innovación responsable aplicada a los productos sanitariosLa investigación y la innovación responsables ofrecen un marco ético y operativo para orientar la tecnología sanitaria hacia fines clínicos y socialmente deseables. Sus cuatro ejes —anticipación, reflexividad, inclusión y capacidad de respuesta— invitan a ir más allá del mero cumplimiento normativo y a diseñar considerando quién usará el dispositivo, en qué contextos y qué consecuencias puede tener su adopción a lo largo del tiempo3.
En el ámbito de los productos sanitarios, la investigación y la innovación responsables son coherentes con el marco regulatorio europeo. El Reglamento (UE) 2017/745 (MDR) exige demostrar un balance beneficio-riesgo favorable y cumplir los requisitos generales de seguridad y funcionamiento, lo que se operacionaliza mediante procesos y estándares clave: sistemas de gestión de la calidad (ISO 13485), gestión del riesgo (ISO 14971 y su guía ISO/TR 24971), ingeniería de usabilidad (IEC/UNE-EN 62366-1:2015 y A1:2020), investigación clínica (ISO 14155) e información al usuario (ISO 20417). La investigación y la innovación responsables complementan esta arquitectura incorporando, desde el inicio, preguntas sobre aceptabilidad, equidad e impacto organizativo4–6.
La combinación de ISO 14971 (riesgos) y IEC/UNE-EN 62366-1 (usabilidad) proporciona una vía práctica para anticiparse: definir criterios de aceptación antes de cada iteración, observar el desempeño en tareas críticas y justificar los rediseños con evidencia, manteniendo la trazabilidad entre requisitos, riesgos, tareas y resultados en la documentación técnica5,6.
Finalmente, innovar responsablemente exige considerar la sostenibilidad del ciclo de vida. Los estándares ISO 14040/14044 proporcionan el andamiaje para un análisis de ciclo de vida riguroso, útil para comparar alternativas (materiales, reutilización frente a desechable, embalaje, procesos de limpieza y esterilización, logística y gestión de residuos), identificar puntos críticos y justificar decisiones de ecodiseño con métricas8.
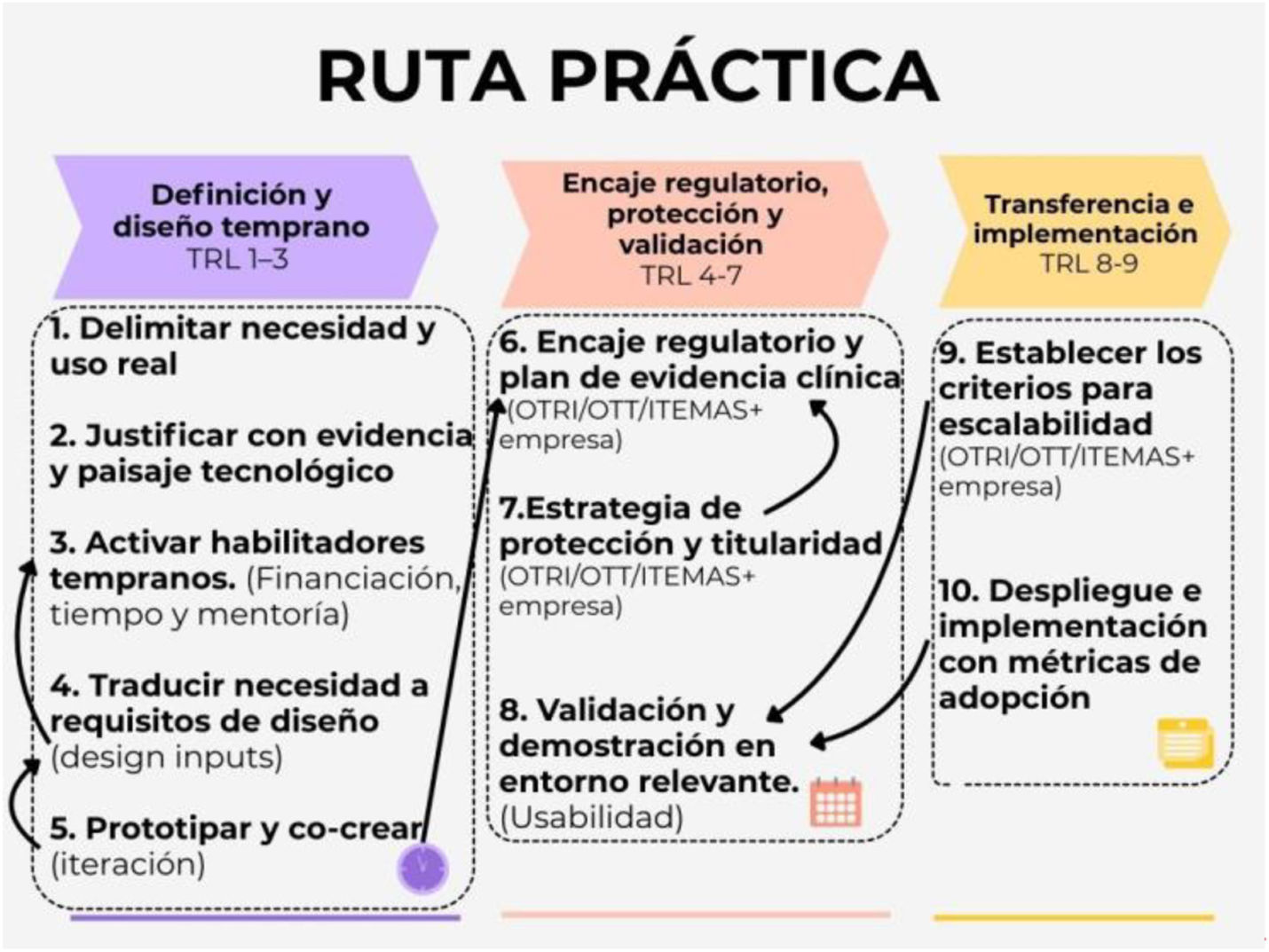
Ruta práctica (10 pasos) para equipos de enfermeríaA continuación, proponemos una ruta práctica en 10 pasos para transformar una necesidad clínica en un producto sanitario transferible, compatible con el entorno del SNS. Esta ruta es orientativa y se recorre de forma iterativa, con retornos frecuentes desde la evaluación y la gestión del riesgo hacia la redefinición del uso previsto, los requisitos y el prototipado (fig. 1).
La ruta arranca con la delimitación del uso real (población, contexto y tareas críticas) y su justificación con evidencia, integrando una revisión del mercado, de la literatura y del paisaje tecnológico y las patentes1. El trabajo de diseño se traduce en establecer los requisitos y cocrear interprofesionalmente prototipos iterativos y, cuando sea pertinente, incluir a pacientes o cuidadores, con criterios éticos y de representatividad, e integrando la sostenibilidad desde fases tempranas2,8. En paralelo se define el encaje regulatorio (finalidad prevista, clasificación y plan de evidencia) y se planifica una evaluación proporcional mediante gestión de riesgos (ISO 14971) e ingeniería de usabilidad (IEC/UNE-EN 62366-1:2015 y A1:2020)4–6. En este punto es clave diferenciar la protección de la innovación, así como considerar la titularidad y evitar divulgaciones prematuras9.
Esta ruta resalta la importancia de un proceso de codesarrollo: clarifica el rol del equipo clínico (necesidad, uso previsto, criterios de aceptación y evidencia) frente al de los fabricantes o centros tecnológicos (industrialización y escalado), articulado con OTRI/OTT y redes de transferencia del SNS9. La validación incluye usabilidad formativa (iteración) y sumativa (validación con diseño fijado, clave para marcado CE), así como generación de evidencia clínica proporcional cuando corresponda6,7. El despliegue se acompaña de métricas de implementación, adopción y valor (seguridad, experiencia/satisfacción, eficiencia y costes) que faciliten su implementación y escalado en el sistema sanitario7,9.
Como limitaciones, cabe señalar que esta guía es orientativa; requiere adaptación a recursos, soporte institucional y nivel de riesgo/clase.
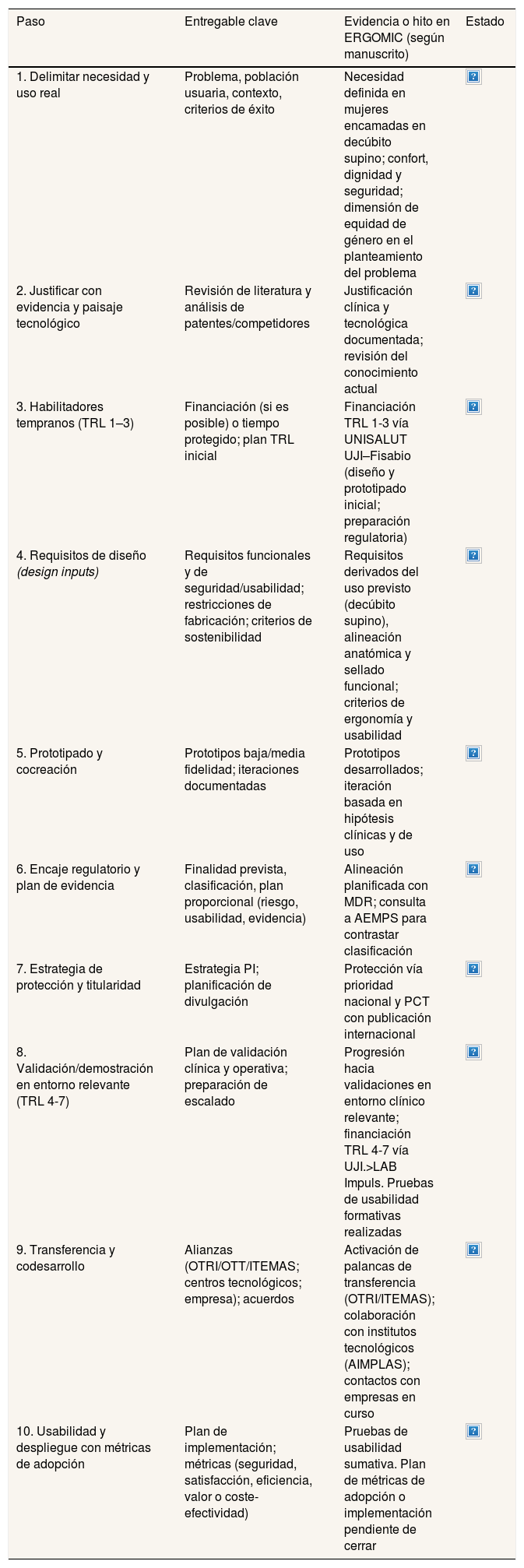
Caso ilustrativo: dispositivo de micción para mujeres en decúbito supino (ERGOMIC)La tabla 1 sintetiza la aplicación de la ruta propuesta para ERGOMIC10, vinculando cada paso con sus entregables principales y con la evidencia o hito generados en el proyecto.
Caso ilustrativo ERGOMIC
| Paso | Entregable clave | Evidencia o hito en ERGOMIC (según manuscrito) | Estado |
|---|---|---|---|
| 1. Delimitar necesidad y uso real | Problema, población usuaria, contexto, criterios de éxito | Necesidad definida en mujeres encamadas en decúbito supino; confort, dignidad y seguridad; dimensión de equidad de género en el planteamiento del problema | |
| 2. Justificar con evidencia y paisaje tecnológico | Revisión de literatura y análisis de patentes/competidores | Justificación clínica y tecnológica documentada; revisión del conocimiento actual | |
| 3. Habilitadores tempranos (TRL 1–3) | Financiación (si es posible) o tiempo protegido; plan TRL inicial | Financiación TRL 1-3 vía UNISALUT UJI–Fisabio (diseño y prototipado inicial; preparación regulatoria) | |
| 4. Requisitos de diseño (design inputs) | Requisitos funcionales y de seguridad/usabilidad; restricciones de fabricación; criterios de sostenibilidad | Requisitos derivados del uso previsto (decúbito supino), alineación anatómica y sellado funcional; criterios de ergonomía y usabilidad | |
| 5. Prototipado y cocreación | Prototipos baja/media fidelidad; iteraciones documentadas | Prototipos desarrollados; iteración basada en hipótesis clínicas y de uso | |
| 6. Encaje regulatorio y plan de evidencia | Finalidad prevista, clasificación, plan proporcional (riesgo, usabilidad, evidencia) | Alineación planificada con MDR; consulta a AEMPS para contrastar clasificación | |
| 7. Estrategia de protección y titularidad | Estrategia PI; planificación de divulgación | Protección vía prioridad nacional y PCT con publicación internacional | |
| 8. Validación/demostración en entorno relevante (TRL 4-7) | Plan de validación clínica y operativa; preparación de escalado | Progresión hacia validaciones en entorno clínico relevante; financiación TRL 4-7 vía UJI.>LAB Impuls. Pruebas de usabilidad formativas realizadas | |
| 9. Transferencia y codesarrollo | Alianzas (OTRI/OTT/ITEMAS; centros tecnológicos; empresa); acuerdos | Activación de palancas de transferencia (OTRI/ITEMAS); colaboración con institutos tecnológicos (AIMPLAS); contactos con empresas en curso | |
| 10. Usabilidad y despliegue con métricas de adopción | Plan de implementación; métricas (seguridad, satisfacción, eficiencia, valor o coste-efectividad) | Pruebas de usabilidad sumativa. Plan de métricas de adopción o implementación pendiente de cerrar |
AEMPS: Agencia Española de Medicamentos y Productos Sanitarios; AIMPLAS: Instituto Tecnológico del Plástico; ITEMAS: Plataforma de dinamización e innovación de las capacidades industriales del Sistema Nacional de Salud; MDR: Medical Device Regulation; OTRI: Servicio de Transferencia de Resultados de Investigación; OTT: Oficina de Transferencia de Tecnología; PCT: Patent Cooperation Treaty; PI: Protección Industrial; TRL: Technology Readiness Levels; UJI: Universitat Jaume I.
Esta ruta aspira a orientar a las enfermeras hacia innovaciones seguras, aceptables y con transferencia viable.
Editor responsable del artículoCarlos Alberto Sánchez Piedra.
Contribuciones de autoríaConceptualización: A. Mesa La Guardia, M.T. Prats Valls, M. Micó Cabedo y J. Gual Ortí. Selección de datos: A. Mesa La Guardia y P. Juan Verdoy. Análisis: A. Mesa La Guardia, J. Gual Ortí y M. Micó Cabedo. Fondos: A. Mesa La Guardia, J. Gual Ortí, M. Micó Cabedo y M.T. Prats Valls. Metodología: A. Mesa La Guardia. Proyecto administrativo: J. Gual Ortí y P. Juan Verdoy. Supervisión de la búsqueda: J. Gual Ortí y P. Juan Verdoy. Validación: A. Mesa La Guardia, J. Gual Ortí, P. Juan Verdoy y N. Domenech Climent. Visualización: A. Mesa La Guardia, J. Gual Ortí y P. Juan Verdoy. Escritura del original: A. Mesa La Guardia, M.T. Prats Valls y M. Micó Cabedo. Revisión del texto: A. Mesa La Guardia, J. Gual Ortí, P. Juan Verdoy y N. Domenech Climent.
AgradecimientosLos autores agradecen a la Universitat Jaume I y a la Fundación para el Fomento de la Investigación Biomédica de la Comunitat Valenciana (Fisabio), por el soporte recibido.
FinanciaciónEste proyecto ha sido financiado por UJILABS IMPULS 2024. Universidad Jaume I.
Conflictos de interesesNinguno.