Realizar un análisis sobre el marco legal de los complementos alimenticios prescritos e indicados para la sintomatología de la menopausia, verificando si de acuerdo con los efectos sobre la salud que producen deben ser considerados como complementos alimenticios o bien en otras categorías recogidas en el ordenamiento jurídico español.
MétodoSe realiza una revisión de los marcos jurídicos aplicables a los complementos alimenticios utilizados en España y Europa, recogiendo aquellos aspectos que resulten aplicables o relevantes para los utilizados durante la menopausia, y la relación que guarden con conceptos jurídicos como la definición de medicamento de uso humano, medicamento a base de plantas medicinales o los denominados «productos frontera».
ResultadosExiste una gran cantidad de productos que pueden ser considerados «productos frontera» y pueden encajar en categorías de productos diferentes, ya que algunas de las plantas en su formulación también se encuentran autorizadas para su uso como medicamentos industriales o medicamentos de plantas medicinales tradicionales.
ConclusionesExisten complementos alimenticios para la menopausia que suscitan dudas razonables sobre su inclusión en otras categorías legales, tanto como medicamentos de uso humano o como medicamentos a base de plantas, por lo que el legislador necesitaría habilitar mecanismos más agiles y revisiones más frecuentes de las nuevas certezas que la ciencia encuentre, y que pueda cambiar la consideración de estos productos.
To analyze the legal framework for the marketing of specific food supplements prescribed and indicated for menopause symptoms, so that it is verified if according to the effects on health that they produce, should be considered in the category of food supplements, or in others included in our legal system.
MethodAn exhaustive review of the legal frameworks applicable to food supplements used both in Spain and in Europe, collecting those aspects that are related to legal concepts such as the definition of medicine for human use, medicine based on medicinal plants, or the so-called “frontier products”.
ResultsThere is a large number of products that can be called “frontier products”, they can fit into different product categories, they can fit into different product categories, since some of the plants in their formulation are also authorized for use as industrial medicines or medicines based on traditional medicinal plants.
ConclusionsThere are currently specific food supplements for menopause that raise reasonable doubts about their inclusion in other legal categories, both as medicines for human use, or as herbal medicines, so the legislator would need to enable more agile mechanisms and more frequent reviews of the new certainties that science finds, and that can change the status of these products.
La menopausia es una etapa vital de la vida que ocupa un tercio de esta, y en ella ocurren múltiples cambios biológicos y psicológicos, por lo que algunas mujeres la perciben como una etapa de disminución en su calidad de vida1, trasciende los efectos naturales que produce e impacta sobre el modo en que se construyen sus relaciones familiares o sociales2.
Esta «crisis vital» transcurrirá conforme a sus valoraciones culturales, resolviéndola cada mujer de acuerdo con su historia personal y su entorno social en ese momento1. Los síntomas asociados a la menopausia pueden aparecer con diversas intensidad y frecuencia. Para algunas mujeres serán casi ausentes, mientras que para otras pueden resultar limitantes3; unos aparecerán a corto plazo, como los síntomas neurovegetativos (sofocos, hormigueo, palpitaciones, insomnio, etc.), y otros a medio plazo (sequedad de la piel y mucosas, atrofia urogenital, etc.) o a largo plazo (osteoporosis y síndrome metabólico).
Para el abordaje de los síntomas están disponibles en el mercado numerosos preparados, con la denominación de «complementos alimenticios», que incluyen una heterogénea cantidad de nutrientes, muchos de ellos usados tradicionalmente para su tratamiento4.
El debate sobre la consideración de las plantas medicinales como medicamentos está abierto desde hace tiempo, pues resulta obvio que en ocasiones presentan usos terapéuticos, de suplementación de la dieta o incluso fines fruitivos4. El auge observado en los últimos años por lo «natural» y los estilos de vida y de alimentación saludables hace que los consumidores se sientan atraídos hacia productos naturales con connotaciones sanitarias, optando por el uso de complementos alimenticios, cosméticos, biocidas y alimentos funcionales, desde la necesidad de satisfacer carencias en nutrientes o bien como apoyo a estilos de vida saludables. La aparición de estos productos en las farmacias comunitarias provoca un problema jurídico de primer orden, ya que su definición legal se hace difusa en su consideración o no como medicamento, y puede suscitar dudas de las normas que les son aplicables5. La recomendación y la dispensación de complementos alimenticios específicos para la menopausia pueden partir de diferentes supuestos: por prescripción médica, a demanda de las usuarias o bien por indicación farmacéutica. En todos ellos, tanto los médicos como los farmacéuticos deben ser conocedores del marco legal que ampara la comercialización de estos productos, pues la inclusión de plantas medicinales hace que deban o puedan tener la consideración de medicamentos6. Resulta conveniente realizar un análisis sobre el marco legal de comercialización de los complementos alimenticios específicos prescritos e indicados para la sintomatología de la menopausia, de manera que se verifique si, de acuerdo con los efectos sobre la salud que producen, deben ser considerados en la categoría de complementos alimenticios o bien en otras recogidas en el ordenamiento jurídico español, puesto que no existen revisiones de ningún tipo publicadas que arrojen luz sobre el tema que nos ocupa.
Método y resultadosSe ha realizado una revisión bibliográfica de los marcos jurídicos aplicables a los complementos alimenticios utilizados tanto en España como en Europa, ya sean prescritos o indicados, recogiendo los aspectos que resulten aplicables o relevantes para aquellos complementos específicos utilizados, indicados o prescritos durante la menopausia, además de la relación que puedan guardar con conceptos jurídicos como la definición legal de medicamento de uso humano, medicamento a base de plantas medicinales o los denominados «productos frontera».
La búsqueda bibliográfica se realizó en las bases de datos PubMed y Google Scholar, y además se buscaron las leyes, reales decretos, reglamentos y directivas más recientes. Los términos incluidos fueron “menopausia”, “legislación”, “complemento alimenticio”, “medicamento a base de plantas”, “medicamento” y “productos frontera”. Como criterio de inclusión se tuvo en cuenta que los artículos fueran lo más recientes posible, entre los años 2005 y 2021, o los más relevantes en el área a estudiar. En el caso de las leyes, reales decretos, reglamentos y directivas, se incluyeron los últimos en vigor.
Marco jurídico de los complementos alimenticios en EspañaLos complementos alimenticios son productos que tienen un tratamiento jurídico muy distinto del de cualquier otro producto sanitario o medicamento, pues en la práctica resultan muy difíciles de distinguir de estos5. Según la legislación de la Unión Europea en materia alimentaria, tienen la consideración de alimentos, según el Reglamento (CE) n.° 178/2002. Su definición viene recogida en la Directiva 2002/46/CE que establece que son «aquellos productos cuyo fin sea complementar la dieta normal, consistentes en fuentes concentradas de nutrientes o de otras sustancias que tengan un efecto nutricional o fisiológico, en forma simple o combinada, comercializados en forma dosificada, es decir, cápsulas, pastillas, tabletas, píldoras y otras formas similares, bolsitas de polvos, ampollas de líquido, botellas con cuentagotas y otras formas similares de líquidos y polvos que deben tomarse en pequeñas cantidades unitarias»7.
La Directiva 2002/46/CE recoge en sus Anexos I y II las vitaminas y los minerales que pueden formar parte de ellos, que podrán ir solos o acompañados de otras sustancias según lo dispuesto en el artículo 2.a de la Directiva 2002/46/CE, que recoge la posibilidad de que incluyan «otras sustancias que tengan un efecto nutricional o fisiológico», como plantas y elementos vegetales, aminoácidos, ácidos grasos esenciales, polisacáridos y probióticos, entre otros5. La transposición de la Directiva 2002/46/CE a la legislación española se tradujo en el R.D. 1487/2009, que articula todo lo referente a definición, fabricación, composición, etiquetado, presentación y publicidad, registro, comercialización y régimen sancionador, de manera que los aspectos más relevantes serán:
- •
Fabricación: en el artículo 2.1 se recoge la limitación en la fabricación a que presenten en su composición exclusivamente las vitaminas y los minerales enumerados en los anexos de este, de una manera positiva y cerrada, impidiendo la inclusión de cualquier otro diferente de los enumerados8. Esa interpretación restrictiva generaba una paradoja, pues mientras en España existían limitaciones a la fabricación, era posible la importación de productos procedentes de otros países de la Unión Europea que sí incluían sustancias diferentes, mediante el procedimiento de reconocimiento mutuo, respetándose los artículos 26 y 28 a 37 del Tratado de Funcionamiento de la Unión Europea9.
- •
Composición: los complementos alimenticios se caracterizan en función de las cantidades máximas recomendadas, las cuales determinan en muchos casos que para un determinado mineral o vitamina las mayores cantidades los convierten en medicamentos, puntualizando que no se les exige ninguna finalidad específica más allá de la que se les presupone, que es complementar la dieta. Se dispuso mediante la directiva 2002/46/CE la definición de las cantidades máximas y mínimas, recogidas en los Anexos I y II, mediante consulta con los Estados miembros y las partes interesadas, aunque actualmente no se ha alcanzado ningún consenso por su complejidad y disparidad de criterios. Esto provoca que la clasificación varíe en los diferentes Estados entre medicamento o complemento alimenticio de una manera muy dispar10. En España, el R.D. 1487/2009 estableció en su Anexo las vitaminas y los minerales autorizados para la elaboración de complementos alimenticios, según los informes del Comité Científico de Alimentación Humana y de la Autoridad Europea de Seguridad Alimentaria; igualmente, su seguridad y las dosis propuestas han sido evaluadas por el Comité Científico de la Agencia Española de Seguridad Alimentaria y Nutrición (AESAN). Este Anexo supuso la ampliación de lo publicado en el R.D. 1275/2003, el R.D 1487/2009 y el R.D 130/2018.
- •
Etiquetado: la información que debe recogerse en el etiquetado viene dispuesta en el artículo 6 de la Directiva 2002/46/CE y debe cumplir unos requisitos mínimos establecidos. Resulta relevante lo dispuesto en su apartado 2: «La etiqueta, presentación y publicidad no atribuirá a los complementos alimenticios la propiedad de prevenir, tratar o curar una enfermedad humana, ni se referirá en absoluto a dichas propiedades»; esto correspondería a la definición en negativo del concepto legal de medicamento, pues si adquirieran esta condición automáticamente se elevarían a la categoría de este último5. Además, se añadirán los generales del etiquetado de alimentos que les son aplicables, contenidos en el Reglamento (UE) n.° 1169/2011 sobre la información alimentaria facilitada al consumidor.
- •
Comercialización y publicidad: la comercialización se realiza previa autorización de las autoridades sanitarias, a través de las comunidades autónomas. Para aquellos que se vayan a comercializar en España y procedan de otros Estados miembros, su procedimiento de autorización se dirigirá ante la AESAN8, aplicándose lo dispuesto en la «Disposición adicional única, Cláusula de reconocimiento mutuo», R.D. 130/2018. Comunicados para su autorización, estos pueden comercializarse mediante cualquier canal de venta, tanto en farmacias comunitarias como en herbolarios, tiendas de alimentación o e-commerce. Respecto a la publicidad, la consideración como alimentos hace que queden supeditados a lo dispuesto en la Ley 17/2011 de seguridad alimentaria y nutrición, que en su artículo 44 establece las directrices de las prohibiciones en materia de publicidad para los alimentos: «la aportación de testimonios de profesionales sanitarios o científicos, reales o ficticios, o de pacientes reales o supuestos, como medio de inducción al consumo, así como la sugerencia de un aval sanitario o científico», así como «la promoción del consumo de alimentos con el fin de sustituir el régimen de alimentación o nutrición comunes, especialmente en los casos de maternidad, lactancia, infancia o tercera edad», además de «la referencia a su uso en centros sanitarios o a su distribución a través de oficinas de farmacia»11.
Para el tratamiento de la menopausia encontramos una amplia gama de complementos alimenticios que vienen siendo usados para suplementar la dieta de las mujeres. Las vitaminas que suelen aparecer en ellos suelen ser la C (relacionada con el cansancio y la fatiga) y las del grupo B, como la B12 (que contribuye al metabolismo energético) y las B5 y B6 (que contribuyen al rendimiento intelectual y la regulación de la actividad hormonal).
Los complementos alimenticios usados en la menopausia se caracterizan además por incluir en su composición otros elementos en virtud del artículo 2a de la Directiva 2002/46/CE, como partes de plantas y elementos vegetales, aminoácidos, ácidos grasos esenciales, polisacáridos y probióticos, entre otros, siendo lo más común partes de plantas o elementos vegetales con usos en menopausia, mientras que mediante el RD 130/2018 se limitó el número de sustancias que se podían utilizar a las recogidas en sus anexos, ante la falta de armonización por parte de los Estados miembros. Entre las plantas más comunes que se suelen incluir en los complementos comercializados aparecen las hojas de salvia o sus sunidades floridas, isoflavonas de soja en extracto enólico, rizoma de cimicífuga racemosa, sauzgatillo, aceite de onagra, raíz de valeriana, lúpulo, pasiflora, rodiola, melatonina e incluso hipérico, utilizado este último para la depresión, el insomnio y la irritabilidad. La inclusión de estas plantas puede suscitar dudas entre prescriptores, dispensadores y usuarias sobre la categoría de estos productos. Jurídicamente, su inclusión hace que se puedan considerar como «productos frontera», término acuñado para aquellos que podrían encajar en diferentes categorías legales, como medicamentos para uso humano, complementos alimenticios, productos cosméticos, productos de cuidado personal, equipos de protección individual y productos de consumo12, y al que se hizo mención por primera vez en la Directiva 2004/24/CE: «(…) el número creciente de productos denominados “frontera” entre el sector de los medicamentos y los demás sectores, resulta conveniente modificar la definición de medicamento para evitar dudas sobre la legislación aplicable cuando un producto responda plenamente a la definición de medicamento pero pudiera responder también a la definición de otros productos regulados».
Este término no supone la aparición de una nueva categoría de productos, ni tampoco se puede aplicar a aquellos que no resultan medicamentos, ya que estos ya tienen su categoría y régimen jurídico propio, sino que es acuñado para recoger la realidad de nuevos productos que se encuentran en áreas limítrofes entre las diferentes categorías como consecuencia de insuficiencias en las definiciones legales recogidas en el ordenamiento jurídico español12.
Consideración como medicamentosAl encontrarnos, pues, ante complementos alimenticios que incluyen en su composición elementos que producen efectos fisiológicos, debemos hacer un análisis de la definición o concepto legal de «medicamento» para identificar si estos productos pueden someterse a su régimen jurídico. La definición legal de «medicamento» se recogió en el artículo 1 de la Directiva 2001/83 del Parlamento Europeo y del Consejo, por la que se establece un código comunitario sobre medicamentos para uso humano, al que los Estados miembros armonizaron su ordenamiento jurídico. Este artículo definía la concepción básica asumible para los medicamentos, junto a otros conceptos complementarios necesarios para su interpretación. Estos conceptos han sido modificados o complementados por otras directivas posteriores, la Directiva 2004/24/CE, la Directiva 2004/27/CE, el Reglamento (CE) n.° 1394/2007 y la Directiva 2011/62/UE, lo que nos da una idea de que la interpretación de la definición de «medicamento» no ha sido pacífica, necesitando aclaraciones por parte de la Comisión Europea y mediante cuestiones prejudiciales que el Tribunal de Justicia de la Unión Europea ha resuelto ayudando también a completar la definición legal del medicamento5. En la legislación española viene recogido en la Ley 29/2006, modificada por el Real Decreto Legislativo 1/2015, por el que se aprueba el texto refundido de la Ley de garantías y uso racional de los medicamentos y productos sanitarios. El artículo 8 de este Real Decreto enumera y delimita de forma expresa los productos que alcanzarán la categoría de medicamentos en:
- •
Medicamentos de uso humano y de uso veterinario elaborados industrialmente.
- •
Fórmulas magistrales.
- •
Preparados oficinales.
- •
Medicamentos especiales previstos en esta ley.
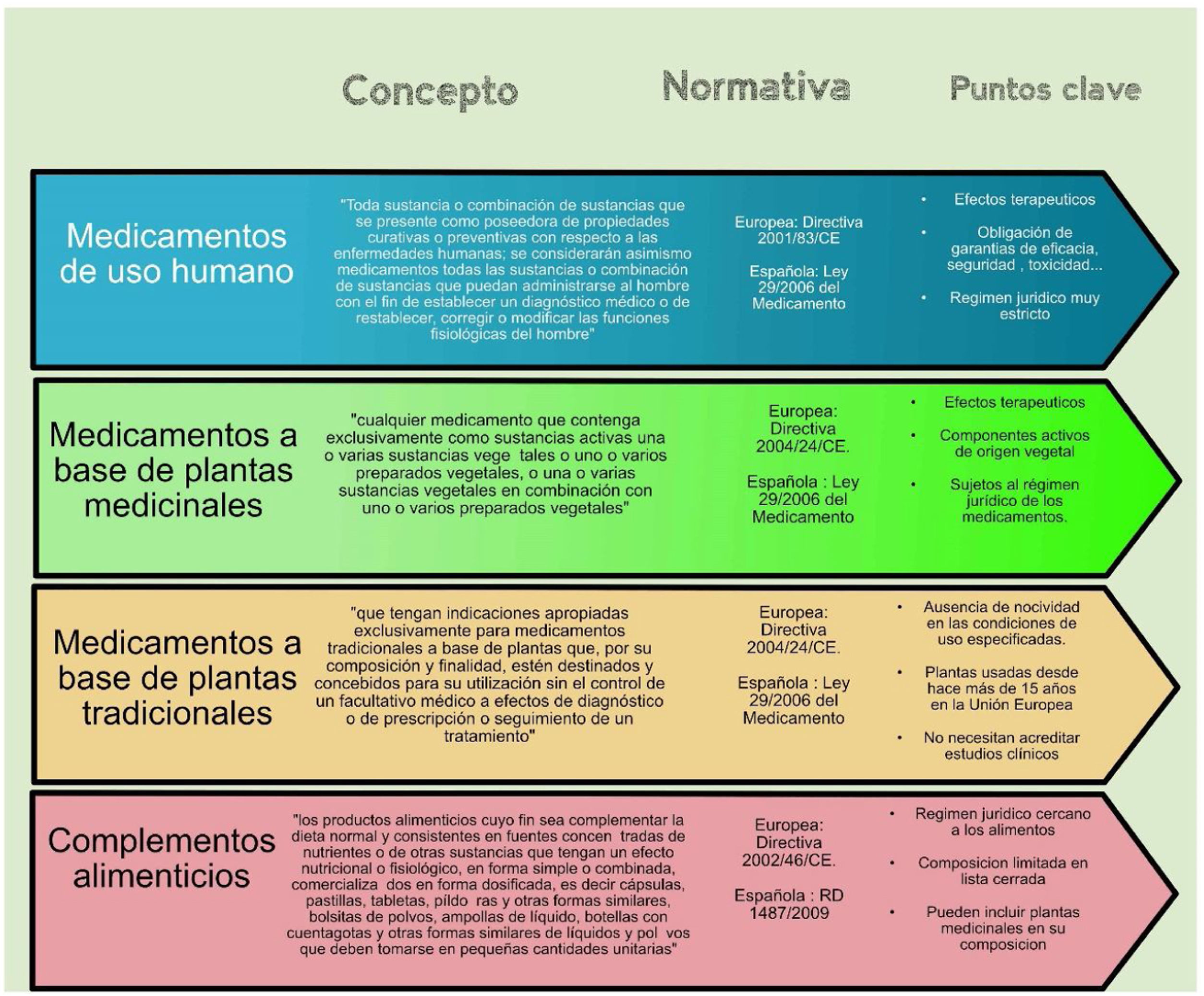
La definición definitiva de «medicamento» en la legislación española recoge como concepto «medicamento de uso humano» (fig. 1) refiriéndose a «toda sustancia o combinación de sustancias que se presente como poseedora de propiedades para el tratamiento o prevención de enfermedades en seres humanos (...) con el fin de restaurar, corregir o modificar las funciones fisiológicas ejerciendo una acción farmacológica, inmunológica o metabólica, o de establecer un diagnóstico médico»13. De manera accesoria también incluye el concepto de «principio activo» o «sustancia activa» como «toda sustancia o mezcla de sustancias destinadas a la fabricación de un medicamento y que, al ser utilizadas en su producción, se convierten en un componente activo de dicho medicamento destinado a ejercer una acción farmacológica, inmunológica o metabólica con el fin de restaurar, corregir o modificar las funciones fisiológicas, o de establecer un diagnóstico»13. Según estos conceptos, podemos considerar las plantas incluidas en los complementos como medicamentos. Un caso singular de esta interpretación es el uso de la cimicífuga racemosa, autorizada por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) como medicamento (Remifemin®) a la par que en complementos alimenticios para la menopausia, igual que otras plantas utilizadas en otros preparados, como el lúpulo, el sauzgatillo o las isoflavonas de soja, entre otras, haciéndose necesario establecer un criterio para la consideración del régimen jurídico aplicable en uno u otro sentido. La paradoja de la convivencia en el mercado de productos que pertenecen a categorías legales distintas se puso de relieve con la cimicífuga racemosa, que fue objeto de la emisión de una alerta sanitaria por posible aparición de daño hepático, realizando recomendaciones a seguir para aquellos medicamentos autorizados, sin hacer referencia a aquellos otros productos que también la incluían en su composición, lo que permitió que estos escaparan a dichas recomendaciones. La eficacia de la cimicífuga racemosa ha sido evaluada por el comité científico de la AESAN, como se pone de relieve en el informe AESAN-2021-016, en el que se recoge su eficacia en el tratamiento de los síntomas menopáusicos formulada como medicamento en comparación con placebo; sin embargo, esta evidencia no ha sido establecida y evaluada para aquellos complementos alimenticios que la incluyen en su formulación.
Analizando el concepto de medicamento bajo el prisma sostenido por el aforismo jurídico in claris non fit interpretatio14, los extractos o las partes de plantas usados en estos complementos contienen sustancias activas, puesto que resulta innegable que realizan una «acción farmacológica, inmunológica o metabólica con el fin de restaurar, corregir o modificar las funciones fisiológicas»13. A ello se debe sumar que el régimen jurídico de los medicamentos ejerce una vis atractiva5 en virtud del principio general de primacía de la protección de la salud pública en la legislación española, donde el artículo 7.6 de la Ley 26/2009 de garantías y uso racional de los medicamentos y productos sanitarios indica: «En caso de duda, cuando un producto pueda responder a la definición de medicamento se le aplicará esta Ley, incluso si a dicho producto se le pudiera aplicar la definición contemplada en otra norma»15. La finalidad de este artículo es aportar una mayor seguridad para identificar el régimen jurídico de un determinado producto, aplicándole siempre el más restrictivo y garantista5. Como ampliación del concepto de «medicamento» se incluyó el de «medicamento a base de plantas medicinales». La presencia de plantas en los complementos usados en la menopausia nos lleva a considerar la posibilidad de un encaje en este concepto concreto. La definición de medicamentos a base de plantas se recogió en la Directiva 2004/24/CE. En la legislación española se encuentra en el artículo 51 de la Ley 26/2009, que establece: «Las plantas y sus mezclas, así como los preparados obtenidos de plantas en forma de extractos, liofilizados, destilados, tinturas, cocimientos o cualquier otra preparación galénica que se presente con utilidad terapéutica, diagnóstica o preventiva seguirán el régimen de las fórmulas magistrales, preparados oficinales o medicamentos industriales, según proceda y con las especificidades que reglamentariamente se establezcan»15. Lo relevante de este concepto resulta del reenvío que realiza al régimen jurídico de los medicamentos, de lo que deducimos que todos aquellos preparados vegetales que presenten características propias de los medicamentos serán remitidos a este régimen jurídico siempre y cuando sean preparados industrialmente o bien como fórmula magistral en las oficinas de farmacia5.
El R.D. 1345/2007, por el que se regula el procedimiento de autorización, registro y condiciones de dispensación de los medicamentos de uso humano fabricados industrialmente, vino a introducir la categoría de medicamentos a base de plantas tradicionales como consecuencia de la transposición de la Directiva 2001/83/CE, categoría con requisitos propios de los medicamentos, que podrán autorizarse mediante un procedimiento simplificado de evaluación y registro. Sin perjuicio de lo dispuesto en el artículo 51 de la Ley 26/2009, para la obtención de la autorización por procedimiento abreviado estos medicamentos deben cumplir los requisitos establecidos. Este procedimiento abreviado los exime de la obligación de realizar pruebas preclínicas y clínicas para acreditar la eficacia y la seguridad de su uso15, permitiendo su comercialización siempre que se ofrezcan sin referencia a propiedades terapéuticas, diagnósticas o preventivas, ya que de hacerlo así y no estar registrados serían considerados medicamentos ilegales5. Los complementos alimenticios fueron regulados por la Directiva 2002/46/CE, que los acerca al tratamiento jurídico que se da a los alimentos, y deben cumplir las funciones que se les atribuyen, suplementar la dieta en situaciones concretas o de una forma general, por lo que, de acuerdo con su marco legal y todo lo expuesto referente a los regímenes de los medicamentos de uso humano y a base de plantas, la inclusión de plantas medicinales en su formulación debería transformarlos en medicamentos a base de plantas, dejando atrás el régimen jurídico como alimento.
DiscusiónLos complementos alimenticios utilizados para el tratamiento de la menopausia son productos formulados que cumplen con el ordenamiento jurídico establecido para estos, aunque con diferencias en cuanto a composición, fabricación, autorización, etiquetado y publicidad entre los Estados miembros de la Unión Europea, siendo en España llamativo que el hecho de la no alusión a sus propiedades en el etiquetado genere una puerta para la inclusión de plantas que, atendiendo a las definiciones que establece la Ley 26/2009 para plantas medicinales o plantas medicinales de uso tradicional, tienen la consideración legal de medicamentos industriales13, que son autorizadas por la AEMPS y están sujetas a los controles de eficacia y seguridad establecidos para los medicamentos industriales.
Por lo tanto, la inclusión de plantas en los productos utilizados para paliar los síntomas de la menopausia puede llevar a dudas sobre la categoría de estos productos dentro del ámbito de alimentos o de medicamentos, bien por la forma de uso tradicional o por las acciones fisiológicas que desencadenan sus componentes. Este hecho plantea un serio problema al aplicar la normativa que los regula, ya que pueden considerarse como «productos frontera». Al encontrarnos ante complementos alimenticios que incluyen en su composición elementos que producen efectos fisiológicos, debemos hacer un análisis de la definición o concepto legal de «medicamento» para identificar si estos productos pueden someterse a su régimen jurídico, como hicieron en el estudio observacional descriptivo de Prieto-Muños y Vidal-Miñada16, en 2021, a través de la revisión caso a caso basándose en la definición completa de cada producto establecida en la legislación nacional y de la Unión Europea considerando los aspectos que diferencian a cada categoría, con el cual consiguieron detectar errores de clasificación o fraudes por la intención de obviar los trámites de autorizaciones más estrictas de los medicamentos respecto a alimentos, productos sanitarios y cosméticos cuya comercialización es más económica y sencilla, constituyendo un problema prioritario de salud pública.
Esta paradoja quedó patente con la cimicífuga racemosa, la cual fue objeto de una alerta sanitaria que resultó aplicable solo a aquellas formas farmacéuticas con condición legal de medicamento, escapando su alcance de los complementos alimenticios. Además, se han seguido estudiando nuevas implicaciones terapéuticas de la cimicífuga racemosa a través de los efectos metabólicos, ya que contiene sustancias activas17 y de hecho realiza una «acción farmacológica, inmunológica o metabólica con el fin de restaurar, corregir o modificar las funciones fisiológicas»13. En España se comercializan preparados con cimicífuga racemosa en formatos tanto de medicamentos a base de plantas como de complementos alimenticios18. Sin embargo, la obtención de la autorización de medicamentos a base de plantas exime de la obligación de realizar las pruebas preclínicas y clínicas necesarias para acreditar su eficacia y seguridad de su uso15.
Los sanitarios deben ser conocedores de la realidad jurídica de este tipo de productos, que aun siendo considerados alimentos seguros debería monitorizarse también su uso, pues la inclusión de las mismas plantas medicinales en dos formatos distintos (medicamentos a base de plantas o complementos alimenticios) hace necesario el ejercicio de un seguimiento terapéutico y una farmacovigilancia para detectar episodios sospechosos, ejercicio que se debería hacer desde las farmacias comunitarias, que son establecimientos sanitarios con profesionales cualificados para llevar a cabo estas acciones, al contrario que otros establecimientos físicos u online en los que se pueden comercializar estos productos.
Las consumidoras, a su vez, deben ser informadas de manera clara y concisa, o al menos disponer de la información necesaria en los casos en que no intervenga ningún profesional sanitario, mediante un etiquetado y una publicidad claros y completos de los complementos, que brinden conocimiento del tipo de productos ante los que se encuentran, de modo que puedan considerar, una vez informadas, la necesidad o no de este tipo de complementos.
En el ánimo del legislador en la elaboración de estas normas se encuentra siempre presente la protección de la salud, en principios de seguridad y eficacia. Este espíritu puede verse comprometido ante eventuales problemas de seguridad si se permite el uso de plantas medicinales en productos que tengan un régimen jurídico diferente del de los medicamentos industriales, incluso si estas plantas tradicionalmente se han considerado seguras, ya que el dinamismo de la ciencia puede cambiar certezas y realizar hallazgos que produzcan cambios en la consideración de las plantas, siendo necesaria la articulación de mecanismos para que el legislador pueda resolver ágilmente los problemas jurídicos que surjan a la misma velocidad con que avanza la industria farmacéutica.
ConclusionesLos complementos alimenticios específicos para la menopausia pueden llevar a dudas sobre su inclusión en la categoría legal de medicamentos de uso humano o en la de medicamentos a base de plantas, siendo necesario que el legislador habilite mecanismos más ágiles y revisiones más frecuentes de los avances de la ciencia, y que pueda cambiar la categoría de estos productos.
Disponibilidad de bases de datos y material para réplicaLos datos están disponibles solicitándolos al Grupo de Investigación de Atención Farmacéutica de la Universidad de Granada. Las personas interesadas pueden contactar por correo electrónico (e.firr@go.ugr.es). Las restricciones en los datos utilizados se deben a cuestiones legales de autorización a la difusión de trabajos por parte de terceros.
Son pocos los trabajos realizados sobre la legislación de los complementos alimenticios, principalmente revisiones de la legislación internacional, y no hay ningún análisis para los complementos alimenticios usados en la menopausia.
¿Qué añade el estudio realizado a la literatura?Se aporta una visión sobre cómo los profesionales deben considerar estos productos, revelar las dudas que pueden suscitar y su posible relación o consideración con el estatus de medicamento.
¿Cuáles son las implicaciones de los resultados obtenidos?En la sociedad actual, con un auge del consumo de lo natural, se debe cuestionar el valor de la naturalidad de determinados productos para el tratamiento de los síntomas de la menopausia.
Javier García Amez.
Declaración de transparenciaEl autor principal (garante responsable del manuscrito) afirma que este manuscrito es un reporte honesto, preciso y transparente del estudio que se remite a Gaceta Sanitaria, que no se han omitido aspectos importantes del estudio, y que las discrepancias del estudio según lo previsto (y, si son relevantes, registradas) se han explicado.
Contribuciones de autoríaF.I. Rubio, M.D. Cabezas, M.I. Valverde, F. Martínez y M.J. Zarzuelo son los autores iniciales de la idea, la primera redacción y la revisión bibliográfica del artículo. M.D. Cabezas y M.I. Valverde contribuyeron sustancialmente en la revisión y la edición del manuscrito. F.I. Rubio contribuyó en la escritura, la supervisión y la validación del documento final junto a F. Martínez y M.J. Zarzuelo. Todas las diferencias y correcciones han sido discutidas y consensuadas entre todas las personas firmantes.
AgradecimientosA Julia Rubio Gámez, por su ayuda en la revisión del texto en inglés.
FinanciaciónNinguna.
Conflictos de interesesNinguno.