Describir y analizar desde el punto de vista clínico y epidemiológico un brote de toxiinfección alimentaria en una institución de enfermos psiquiátricos de Granada, en 2015, y examinar si el tratamiento con psicofármacos constituye un factor de riesgo para desarrollar una toxiinfección alimentaria, analizando los grados de susceptibilidad según el grupo terapéutico consumido.
MétodoEstudio ambispectivo de cohortes. La unidad de análisis fueron los residentes. Se realizó búsqueda activa de casos, encuesta alimentaria y búsqueda de otros riesgos, e inspección alimentaria. Se estudiaron variables de persona, lugar y tiempo. Análisis descriptivo (frecuencias absolutas y relativas), cálculo de las tasas de ataque por pabellón y por menú. Análisis bivariado (ji al cuadrado, t de Student) y riesgo relativo como medida de la fuerza de asociación. Análisis multivariado mediante regresión logística para el análisis de riesgos de la medicación.
ResultadosSe contabilizaron 18 casos con diarrea sin fiebre (periodo de incubación de 6-16 horas), de carácter leve y autolimitado. Las manifestaciones clínicas, la agrupación temporal de casos y las características de los alimentos ingeridos centraron la sospecha en una toxina bacteriana. A igualdad en el resto de variables, los grupos terapéuticos N03AF y N03AG confirieron mayor riesgo de enfermar (odds ratio [OR]: 8,626; intervalo de confianza del 95% [IC95%]: 2,050-36,308; p=0,003; y OR: 14,516; IC95%: 3,155-66,784; p=0,001, respectivamente).
ConclusiónLa disminución del tránsito intestinal causada por la administración de antiepilépticos puede aumentar el tiempo de exposición de la mucosa intestinal a la toxina, aumentando el riesgo de enfermar y de padecer complicaciones. Debe realizarse un esfuerzo higiénico suplementario en este tipo de instituciones para prevenir estas afecciones.
To describe and analyse from a clinical and epidemiological point of view, a food borne outbreak in a psychiatric institution in Granada, in 2015, and to examine whether treatment with psychoactive drugs constitutes a risk factor for the development of a food borne disease, analysing the degree of susceptibility according to the therapeutic group consumed.
MethodAmbispective cohort study. Residents were the unit of analysis. Our group carried out an active case search and a food survey. A search for other risks was developed as well as a food inspection. Location, time and individual variables were studied. A descriptive analysis was conducted (absolute and relative frequencies). Calculation of attack rates by building and by menu was made. Bi-variant analysis (Chi-square test, t-Student test) and relative risk were used as a measure of strength of association. For risk analysis of medication, a multivariate analysis using logistic regression was carried out.
Results18 cases with diarrhoea without fever were found (incubation period from 6 to 16hours). Cases were mild and self-limiting. The clinical manifestations, the temporal grouping of cases and the characteristics of the ingested foods, focussed suspicion on a bacterial toxin. Being equal in the rest of variables, the N03AF, and N03AG therapeutic groups confer greater risk of disease (odds ratio [OR]: 8.626; 95% confidence interval [95%CI]: 2.050-36.308; p=0.003; and OR: 14.516; 95%CI: 3.155-66.784; p=0.001, respectively).
ConclusionDecreased intestinal transit, caused by the administration of anticonvulsants, may increase exposure time of the intestinal mucosa to the toxin, increasing the risk of disease and suffering from complications. An additional hygienic effort should be made in this type of institution to prevent these pathologies.
Los alimentos constituyen un soporte activo de contaminación y multiplicación de patógenos. Los cambios en el consumo, el procesado, la transformación y el suministro de alimentos conllevan una mayor manipulación de estos y suponen un riesgo para la salud, contribuyendo a un incremento del número de brotes de enfermedades de origen alimentario1. Entre 2008 y 2011 se produjeron en nuestro país 2342 brotes de enfermedades relacionadas con los alimentos, con 30.219 casos asociados, 1763 hospitalizaciones y 24 defunciones2. Los principales factores que originan toxiinfecciones alimentarias están relacionados con una procedencia no segura del alimento, una elaboración o una exposición a temperatura inadecuadas, un mantenimiento incorrecto o una contaminación cruzada por una higiene deficiente del personal o del equipo utilizado3.
Existen multitud de agentes patógenos implicados en la etiología de estas infecciones. La aparición y la intensidad de los síntomas varía en función del tipo de contaminación, de la cantidad de alimento infectado consumido y de la vulnerabilidad individual4. Algunos grupos poblacionales muestran una mayor probabilidad de enfermar por patógenos vehiculados por la comida, o de desarrollar una presentación clínica de mayor gravedad. Los factores de riesgo tradicionalmente asociados a esta mayor susceptibilidad son la edad, el estado inmunitario, el estado nutricional y la comorbilidad asociada. No obstante, la medicación consumida puede conllevar situaciones de mayor vulnerabilidad, cuyo resultado es una reducción en la dosis infectante necesaria para causar enfermedad5.
Los estudios sobre vulnerabilidad frente a enfermedades infecciosas gastrointestinales por grupos farmacológicos específicos son escasos y se centran sobre todo en el consumo de antidiarreicos, para los cuales se ha establecido un incremento de la gravedad de la infección4.
La identificación del agente causal y del vehículo, y la rápida instauración de medidas preventivas empíricas de contención, son los elementos clave para el control efectivo de un brote. Sin embargo, según el informe del Centro Europeo para la Prevención y Control de Enfermedades, en 2015 tan solo se identificó el agente causal en el 66,5% de los brotes alimentarios ocurridos en la Unión Europea6. A pesar de su escasa utilización, la investigación epidemiológica ha demostrado ser una metodología eficaz en la filiación precoz del agente o del vehículo sospechados7.
El complejo donde se desarrolló el estudio es un centro de financiación mixta (pública y privada) dedicado a la educación, la asistencia, la rehabilitación y la promoción sociolaboral de las personas con discapacidad intelectual. Tiene capacidad para atender a alrededor de 400 personas en seis edificios independientes, tres dedicados a residencia y tres a estancia diurna, todos ellos con comedores propios. Los servicios de cocina están externalizados y las comidas se elaboran en una única cocina de la empresa, ubicada en el mismo complejo. El menú se divide en un menú normal y uno de dieta, que son los mismos para todos los comedores. La comida se traslada en bandejas cubiertas a cada comedor. Posteriormente, en el office del comedor se colocan en soportes calientes tipo samovar (mesas calientes). Las comidas son servidas a los comensales por profesionales auxiliares. Los trabajadores del centro comen en los comedores de lunes a viernes, y el personal de cocina come todos los días (incluido el fin de semana) en la cocina. Sin embargo, únicamente las personas residentes realizan las cenas en los comedores del centro.
En 2012 se produjo, en este centro, un brote de toxiinfección alimentaria que afectó a 42 comensales. De ellos, un afectado requirió ingreso hospitalario y otro tuvo un desenlace fatal a las pocas horas de iniciar la sintomatología. En ese caso, el agente causante fue Clostridium perfringens.
El objetivo de este estudio es describir y analizar, desde el punto de vista clínico y epidemiológico, un brote de toxiinfección alimentaria con similares características, acontecido 3 años después en la misma institución, y examinar si el tratamiento con psicofármacos constituye un factor de riesgo para el desarrollo de una toxiinfección alimentaria, analizando los grados de susceptibilidad según el grupo terapéutico consumido.
MétodoEl mismo día de la aparición de los casos se comunicó la sospecha de brote de toxiinfección alimentaria. Se conformó un grupo de investigación multidisciplinaria y se llevó a cabo una búsqueda activa de casos, un cuestionario alimentario a las personas residentes, una encuesta a las personas encargadas de manipular los alimentos, una inspección de las instalaciones y una revisión de los planes de autocontrol alimentario y de los planes generales de higiene. La hipótesis etiológica inicial, conociendo la distribución del inicio de los síntomas de los casos y sus características clínicas, se orientó a la presencia de una toxina presente en los alimentos ingeridos en la noche anterior a la madrugada de la aparición de los casos. Inicialmente se estableció como definición de caso sospechoso «toda persona del centro que desarrollase síntomas compatibles con gastroenteritis aguda posteriormente a la aparición del primer caso, y que hubiese realizado las comidas en los comedores del centro». Se procedió a la recogida de muestras de heces de siete enfermos y se realizó coprocultivo para investigación de bacterias y de virus entéricos mediante reacción en cadena de la polimerasa (PCR). Se investigó el estado de portador nasal de Staphylococcus aureus en las personas manipuladoras de alimentos y en los/las cocineros/as, mediante cultivo de frotis nasofaríngeo.
Debido a que las personas residentes poseen un déficit cognitivo, la encuesta alimentaria individual no pudo realizarse, pero al ser los menús similares en cada comedor pudo determinarse una aproximación de riesgos de los alimentos, diferenciándose entre menú estándar y dieta. No se pudo obtener muestras de los alimentos al no existir platos testigos.
Se estableció como hipótesis que aquellas personas que consumían determinados psicofármacos presentaban una mayor vulnerabilidad a enfermar de manera sintomática. Con el objeto de verificarla y de estudiar otros posibles factores implicados, se realizó un estudio ambispectivo de cohortes en el cual la unidad de análisis fueron las personas residentes durante el periodo epidémico establecido, considerando que el riesgo de enfermar difería según variables sociodemográficas y la medicación que consumían. Se excluyeron el personal y las personas usuarias que no realizaban las cenas en las dependencias del centro. La cohorte quedó compuesta por 103 residentes.
Las variables de estudio fueron variables de persona: sexo, edad, pabellón (R. Adultos; R. Menores; R. Psicodeficientes, con mayor dependencia [PGD]), tipo de menú (normal o dieta) y consumo de psicofármacos (sí/no); y variables relacionadas con la enfermedad: estado de salud (enfermo/a; sano/a), sintomatología (dolor abdominal, vómitos, diarrea, fiebre, otros) y periodo de incubación. Los datos de consumo se presentan estratificados por subgrupos terapéuticos de la clasificación ATC (Anatomical, Therapeutic, Chemical) instituida por la Organización Mundial de la Salud8. Los fármacos de uso sobre el sistema digestivo y nervioso en nuestra población se clasifican en laxantes osmóticos (A06A), antiepilépticos (N03A), agentes anticolinérgicos (N04A), antipsicóticos (N05A), ansiolíticos (N05B), hipnóticos y sedantes (N05C), antidepresivos (N06A) y psicoestimulantes y nootrópicos (N06B). Se definió como expuesta aquella persona que consumiera algún fármaco de alguno de estos grupos, y como no expuesta a las restantes personas residentes de la cohorte.
Se realizó un análisis descriptivo con cálculo de frecuencias absolutas y relativas, y se calculó la tasa de ataque por pabellón y por menú. Se realizó un análisis bivariado (pruebas de ji al cuadrado, Fisher y t de Student) entre las variables «estado de salud» y cada uno de los diferentes grupos de fármacos, para lo que se calculó el riesgo relativo (RR) como medida de asociación, fijando un nivel de confianza del 95%. Para su cálculo, se sumó 0,5 a todas las frecuencias cuando las variables analizadas no presentaron casos en alguna de sus categorías (enfermos/as no expuestos/as a antiepilépticos). Para evaluar la relación entre la variable «estado de salud» y las demás covariables, se llevó a cabo un ajuste mediante regresión logística, incluyendo los subgrupos terapéuticos. Se utilizó la R2 Nagelkerke para estimar la proporción de variabilidad de la variable dependiente atribuible al conjunto de variables del modelo. Los datos se informatizaron en una base de datos Excel. El análisis estadístico se llevó a cabo con SPSS v.20 y Epidat 3.1.
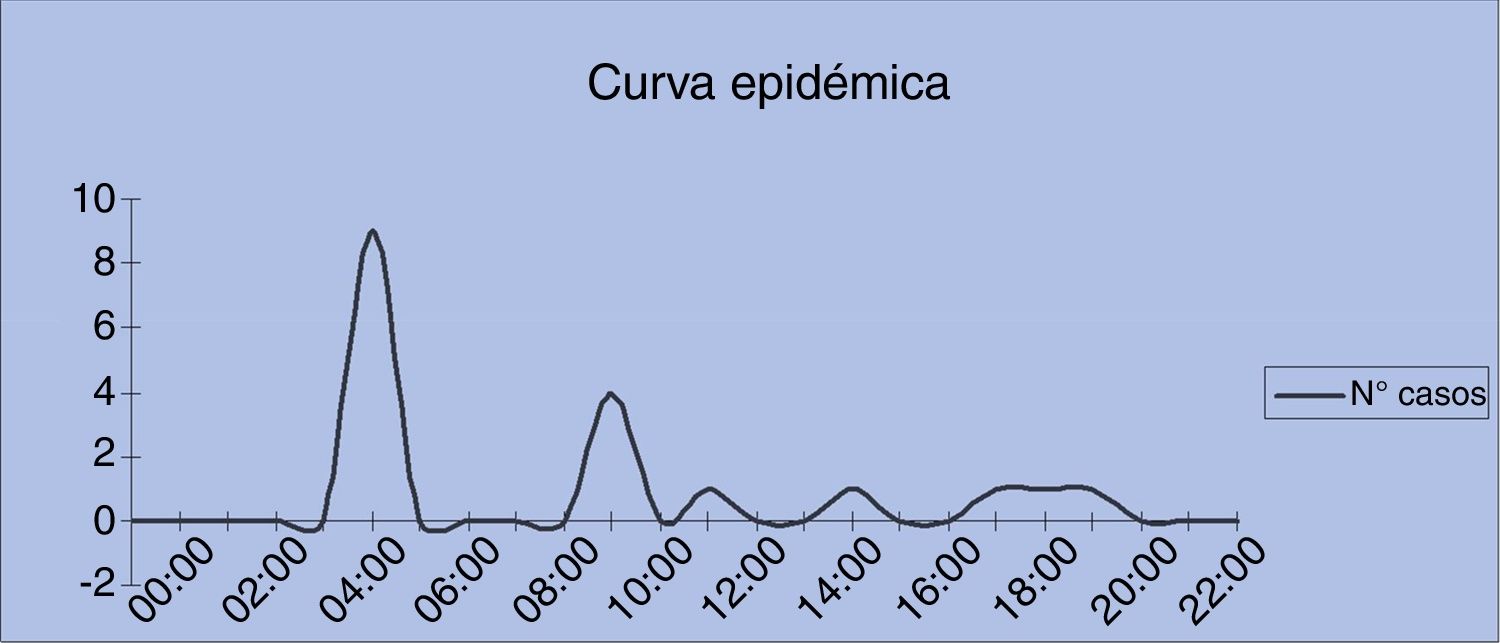
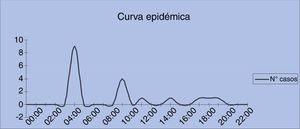
ResultadosSe identificaron 18 personas afectadas, que presentaron dolor abdominal y diarrea, sin productos patológicos, y sin evidencia de otros síntomas. El cuadro fue leve y autolimitado. Debido a la estrecha agrupación de los casos y a la ausencia de fiebre, la sospecha recayó sobre la cena inmediatamente anterior a la aparición de los casos. El periodo medio de incubación fue de 11 horas y la mediana fue de 4 horas (rango: 6-16h). Tras dos periodos máximos de incubación sin notificación de nuevos casos (32h después del primer caso) se dio por finalizado el brote, que finalmente presentó un periodo epidémico de 18 horas (fig. 1).
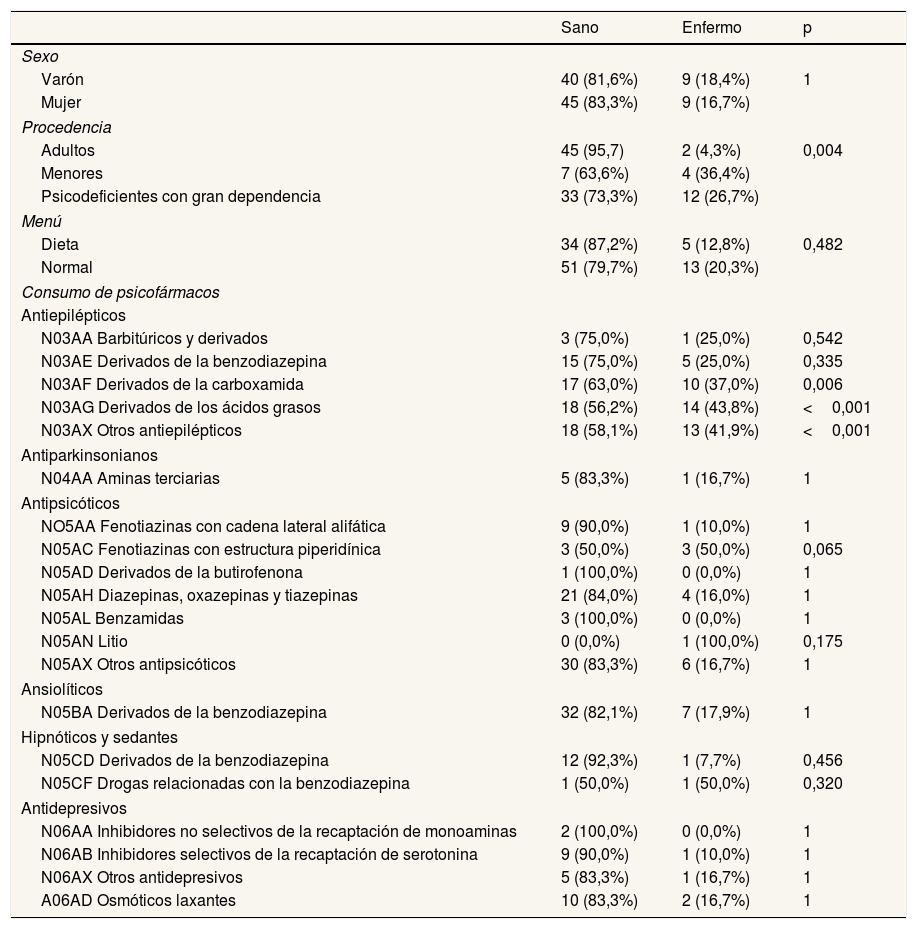
La tasa de ataque general del brote fue del 17,5%. Los casos se distribuyeron en igual proporción entre mujeres y hombres (50%), aunque la tasa de ataque fue ligeramente superior en las mujeres (18,4% frente al 16,7% en los varones). La media de edad de las personas afectadas fue de 30,39 años (rango: 9-66 años), y la mediana fue de 30 años (tabla 1). Los casos se distribuyeron entre los pabellones de adultos (4,3%), PGD (26,7%) y menores (36,4%). El 72,2% consumió el menú estándar. Como se observa en la tabla 2tabla 2, todos los casos consumían medicación antiepiléptica y más de la mitad tomaban medicación antipsicótica. Tan solo dos de los casos (11,1%) tenían prescritos laxantes osmóticos.
Distribución de los factores según estado (enfermo/sano). Análisis bivariado: factores relacionados con el estado
| Sano | Enfermo | p | |
|---|---|---|---|
| Sexo | |||
| Varón | 40 (81,6%) | 9 (18,4%) | 1 |
| Mujer | 45 (83,3%) | 9 (16,7%) | |
| Procedencia | |||
| Adultos | 45 (95,7) | 2 (4,3%) | 0,004 |
| Menores | 7 (63,6%) | 4 (36,4%) | |
| Psicodeficientes con gran dependencia | 33 (73,3%) | 12 (26,7%) | |
| Menú | |||
| Dieta | 34 (87,2%) | 5 (12,8%) | 0,482 |
| Normal | 51 (79,7%) | 13 (20,3%) | |
| Consumo de psicofármacos | |||
| Antiepilépticos | |||
| N03AA Barbitúricos y derivados | 3 (75,0%) | 1 (25,0%) | 0,542 |
| N03AE Derivados de la benzodiazepina | 15 (75,0%) | 5 (25,0%) | 0,335 |
| N03AF Derivados de la carboxamida | 17 (63,0%) | 10 (37,0%) | 0,006 |
| N03AG Derivados de los ácidos grasos | 18 (56,2%) | 14 (43,8%) | <0,001 |
| N03AX Otros antiepilépticos | 18 (58,1%) | 13 (41,9%) | <0,001 |
| Antiparkinsonianos | |||
| N04AA Aminas terciarias | 5 (83,3%) | 1 (16,7%) | 1 |
| Antipsicóticos | |||
| NO5AA Fenotiazinas con cadena lateral alifática | 9 (90,0%) | 1 (10,0%) | 1 |
| N05AC Fenotiazinas con estructura piperidínica | 3 (50,0%) | 3 (50,0%) | 0,065 |
| N05AD Derivados de la butirofenona | 1 (100,0%) | 0 (0,0%) | 1 |
| N05AH Diazepinas, oxazepinas y tiazepinas | 21 (84,0%) | 4 (16,0%) | 1 |
| N05AL Benzamidas | 3 (100,0%) | 0 (0,0%) | 1 |
| N05AN Litio | 0 (0,0%) | 1 (100,0%) | 0,175 |
| N05AX Otros antipsicóticos | 30 (83,3%) | 6 (16,7%) | 1 |
| Ansiolíticos | |||
| N05BA Derivados de la benzodiazepina | 32 (82,1%) | 7 (17,9%) | 1 |
| Hipnóticos y sedantes | |||
| N05CD Derivados de la benzodiazepina | 12 (92,3%) | 1 (7,7%) | 0,456 |
| N05CF Drogas relacionadas con la benzodiazepina | 1 (50,0%) | 1 (50,0%) | 0,320 |
| Antidepresivos | |||
| N06AA Inhibidores no selectivos de la recaptación de monoaminas | 2 (100,0%) | 0 (0,0%) | 1 |
| N06AB Inhibidores selectivos de la recaptación de serotonina | 9 (90,0%) | 1 (10,0%) | 1 |
| N06AX Otros antidepresivos | 5 (83,3%) | 1 (16,7%) | 1 |
| A06AD Osmóticos laxantes | 10 (83,3%) | 2 (16,7%) | 1 |
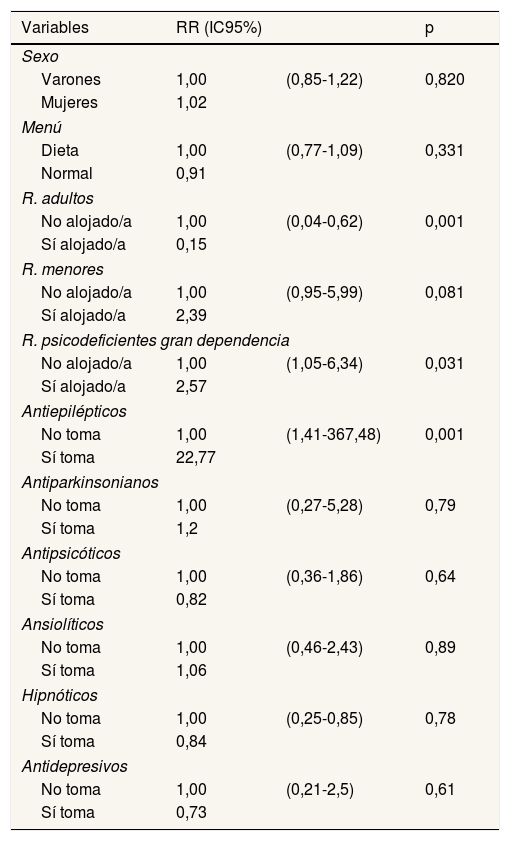
Considerando cada una de las variables de forma independiente, la toma de antiepilépticos (RR: 22,77; IC95%: 1,41-367,48; p=0,001) y la ubicación en el pabellón de PGD (RR: 2,57; IC95%: 1,05-6,34; p=0,031) y en el de menores (RR: 2,39; IC95%: 0,95-5,99; p=0,081) se asociaron a un mayor riesgo de enfermar. Las personas residentes ubicadas en el pabellón de adultos presentaron un menor riesgo de enfermar (RR: 0,15; IC95%: 0,04-0,62; p=0,001) (tabla 3).
Riesgo relativo de enfermar por variables del estudio
| Variables | RR (IC95%) | p | |
|---|---|---|---|
| Sexo | |||
| Varones | 1,00 | (0,85-1,22) | 0,820 |
| Mujeres | 1,02 | ||
| Menú | |||
| Dieta | 1,00 | (0,77-1,09) | 0,331 |
| Normal | 0,91 | ||
| R. adultos | |||
| No alojado/a | 1,00 | (0,04-0,62) | 0,001 |
| Sí alojado/a | 0,15 | ||
| R. menores | |||
| No alojado/a | 1,00 | (0,95-5,99) | 0,081 |
| Sí alojado/a | 2,39 | ||
| R. psicodeficientes gran dependencia | |||
| No alojado/a | 1,00 | (1,05-6,34) | 0,031 |
| Sí alojado/a | 2,57 | ||
| Antiepilépticos | |||
| No toma | 1,00 | (1,41-367,48) | 0,001 |
| Sí toma | 22,77 | ||
| Antiparkinsonianos | |||
| No toma | 1,00 | (0,27-5,28) | 0,79 |
| Sí toma | 1,2 | ||
| Antipsicóticos | |||
| No toma | 1,00 | (0,36-1,86) | 0,64 |
| Sí toma | 0,82 | ||
| Ansiolíticos | |||
| No toma | 1,00 | (0,46-2,43) | 0,89 |
| Sí toma | 1,06 | ||
| Hipnóticos | |||
| No toma | 1,00 | (0,25-0,85) | 0,78 |
| Sí toma | 0,84 | ||
| Antidepresivos | |||
| No toma | 1,00 | (0,21-2,5) | 0,61 |
| Sí toma | 0,73 | ||
IC95%: intervalo de confianza del 95%; RR: riesgo relativo.
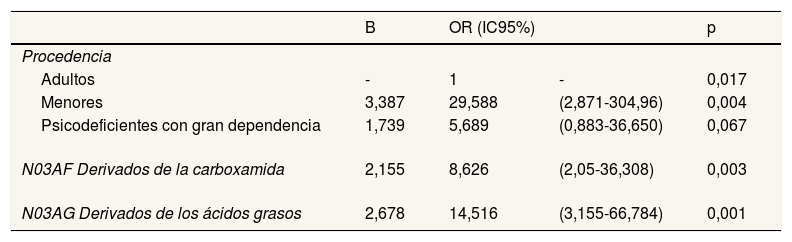
El conjunto de las variables presentes en el modelo pudo explicar el 75,1% de la variabilidad de la variable dependiente «estado de salud». Ajustado el modelo, en la tabla 4 se presentan los resultados obtenidos.
Análisis multivariado, riesgo de enfermar por variables del estudio
| B | OR (IC95%) | p | ||
|---|---|---|---|---|
| Procedencia | ||||
| Adultos | - | 1 | - | 0,017 |
| Menores | 3,387 | 29,588 | (2,871-304,96) | 0,004 |
| Psicodeficientes con gran dependencia | 1,739 | 5,689 | (0,883-36,650) | 0,067 |
N03AF Derivados de la carboxamida | 2,155 | 8,626 | (2,05-36,308) | 0,003 |
N03AG Derivados de los ácidos grasos | 2,678 | 14,516 | (3,155-66,784) | 0,001 |
IC95%: intervalo de confianza del 95%; OR: odds ratio.
Esto permite concluir que, controlado por el efecto del conjunto de las variables, el riesgo de enfermar es 8,626 veces mayor en los sujetos que toman derivados de la carboxamida y 14,516 veces mayor en los que toman derivados de los ácidos grasos. Las personas residentes del pabellón de menores y de PGD tienen 29,588 y 5,689 veces más riesgo de enfermar, respectivamente, que aquellas que se alojan en el de adultos.
Los resultados de los estudios microbiológicos fueron negativos, tanto la investigación de las heces como el estudio de portadores. Se recogieron muestras alimentarias de otros platos que se sirvieron el día anterior, y todas resultaron negativas. Se comprobó que las instalaciones se encontraban en un buen estado de conservación y limpieza aparente, pero el registro de trazabilidad fue deficiente, pudiendo ocasionar errores en la aplicación de medidas cautelares. El procedimiento de muestras testigo tampoco fue adecuado, pues no había muestras de la comida sospechada. Dada la agrupación temporal de los casos, el cuadro clínico y su carácter autolimitado, así como la negatividad de los estudios microbiológicos realizados, se estableció como agente causal a C. perfringens.
DiscusiónLa aparición brusca y la agrupación temporal de los casos centraron la sospecha en un origen común del brote, fortaleciendo la hipótesis de causalidad hacia una toxiinfección alimentaria. La clínica presentada por las personas afectadas (ausencia de fiebre y ausencia de productos patológicos en las deposiciones), así como las características del cuadro (leve y autolimitado), reforzaron la sospecha de la implicación de una toxina bacteriana en la etiopatogenia del brote. Dado que los cuadros alimentarios por toxinas suelen tener periodos de incubación cortos, la sospecha se centró en la cena del día anterior, siendo el alimento vehículo causante más probable la carne, por ser común a los dos tipos de menú. Los resultados de las pruebas de laboratorio no arrojaron ninguna evidencia microbiológica sólida, por lo que en este caso la investigación epidemiológica fue clave para la elaboración del correcto diagnóstico y para la toma subsecuente de medidas de prevención y control adecuadas. Las características clínicas del cuadro, el periodo de incubación (6-16h), el alimento sospechoso (carne) y la negatividad frente a S. aureus en los cultivos de frotis nasofaríngeo de manipuladores/as y de otras pruebas microbiológicas condujeron a señalar como causa de la toxiinfección alimentaria un cuadro toxigénico mediado por C. perfringens.
C. perfringens es una bacteria grampositiva, anaerobia, esporulada y formadora de enterotoxinas, que se encuentra en el ambiente y en el tracto gastrointestinal de los humanos y de animales de consumo humano. Estas toxinas son causa de cuadros clínicos como la gangrena gaseosa, la enteritis necrotizante y toxiinfecciones alimentarias9. Este patógeno está considerado como la tercera causa más común de toxiinfección alimentaria en los países occidentales, siendo el causante de hasta el 10% de los brotes de toxiinfecciones alimentarias ocurridos entre 2008 y 2011 en España2. Produce un cuadro diarreico tras un periodo de incubación que oscila entre 8 y 24 horas (periodo medio: 12h), que se resuelve de manera espontánea a las 24 horas y que se asocia muy frecuentemente con el consumo de alimentos cárnicos almacenados incorrectamente o cocinados a temperaturas inadecuadas, siendo la temperatura óptima de multiplicación del patógeno de 43-47°C10. El diagnóstico se realiza mediante cultivos cuantitativos de heces y de muestras de alimentos implicados, considerándose positivos recuentos superiores al millón de unidades formadoras de colonias. Sin embargo, la prueba diagnóstica de elección es la detección de enterotoxina en las heces11.
Algunos estudios han puesto de manifiesto la gravedad de los brotes de toxiinfección alimentaria por C. perfringens que se desarrollan en instituciones que albergan a personas con diversidad funcional cognitiva. Los resultados de estas investigaciones mostraron que en algunas personas que recibían medicación psiquiátrica se produjeron casos de enteritis necrotizante que resultaron letales12–14. En una de ellas, se apuntaba que el estreñimiento causado por la toma de psicofármacos con potentes efectos anticolinérgicos constituía un factor de riesgo para el desarrollo de este cuadro grave12. El estreñimiento está considerado un problema frecuente en los pacientes con discapacidad intelectual, a pesar del uso de laxantes. Se conjetura que esa situación podría ser el resultado de diversos factores, como la patología cognitiva de base, la inmovilización y el uso de terapias anticonvulsivantes, benzodiacepinas, antagonistas de los receptores H2 o inhibidores de la bomba de protones15. Los antiepilépticos pueden ser una de las medicaciones que con más frecuencia causan estreñimiento16, y este suele ser una de las reacciones adversas frecuentes en dicho grupo terapéutico17–20. En el presente estudio se demuestra, mediante técnicas estadísticas avanzadas, que existe una asociación entre el consumo de ciertos grupos de antiepilépticos (N03AG y N03AF) y el riesgo de enfermar. Los pabellones de menores y de PGD albergan residentes con enfermedades psiquiátricas más complejas y, por tanto, con un mayor consumo de psicofármacos, en especial de antiepilépticos (NO3). Es importante dar a conocer este riesgo identificado en residencias de pacientes psiquiátricos, ya que los planes de higiene y autocontrol deben extremar los puntos críticos que puedan producir brotes alimentarios producidos por toxinas.
Uno de los principales retos de esta investigación fue la falta de muestras de los alimentos consumidos. En las inspecciones de las instalaciones se detectaron defectos en el registro de trazabilidad, pues no quedaban anotados los ingredientes que componían el menú ni el lote de procedencia. No se pudo realizar el estudio microbiológico de la cena del día del incidente al no disponer de platos testigo de esa comida, aunque sí se realizó del resto de las comidas de ese mismo día, siendo todas negativas. Además, no se llevó a cabo la investigación de toxinas alimentarias mediante técnicas directas (PCR) o indirectas (ELISA o aglutinación pasiva reversa por látex) de forma sistemática, por lo que en este caso el diagnóstico se realizó gracias a la evidencia epidemiológica y al descarte de otras enfermedades por los procedimientos microbiológicos habituales.
ConclusiónLa institucionalización, con la consecuente preparación masiva de alimentos, puede favorecer prácticas de manipulación y conservación inadecuadas. El factor más importante identificado es la susceptibilidad de las personas residentes a enfermar por la toma de medicación antiepiléptica, en relación con la disminución de la velocidad del tránsito intestinal y el aumento del tiempo de exposición a la toxina. Es esperable que se incremente el número de personas vulnerables al aumentar la esperanza de vida, las enfermedades crónicas y las situaciones de polimedicación. En estas circunstancias, debe realizarse un esfuerzo suplementario en el sistema de autocontrol y planes de higiene para minimizar el daño en la población institucionalizada.
Los patógenos vehiculizados a través de los alimentos causan infecciones de mayor gravedad en poblaciones vulnerables. Las enfermedades concomitantes, el estado inmunitario, la edad y ciertas medicaciones suelen incrementar la susceptibilidad individual, y en un contexto de restauración colectiva aumentan el riesgo de aparición de brotes graves.
¿Qué añade el estudio realizado a la literatura?Mediante técnicas estadísticas avanzadas se demuestra la asociación existente entre el consumo de ciertos grupos de anticonvulsivantes y el riesgo de enfermar en una población especialmente vulnerable y polimedicada. La investigación epidemiológica se presenta como una herramienta clave para la filiación del agente causal en situaciones que requieren un diagnóstico preciso y rápido por las consecuencias fatales en estas poblaciones cada vez más frecuentes.
Carlos Álvarez-Dardet.
Declaración de transparenciaLa autora principal (garante responsable del manuscrito) afirma que este manuscrito es un reporte honesto, preciso y transparente del estudio que se remite a Gaceta Sanitaria, que no se han omitido aspectos importantes del estudio, y que las discrepancias del estudio según lo previsto (y, si son relevantes, registradas) se han explicado.
Contribuciones de autoríaConcepción y diseño del estudio: B. López-Hernández y A. Corma-Gómez. Recogida de la información: B. López-Hernández, A. Corma-Gómez, M.D. Sánchez Mariscal y R. López-Sepúlveda. Control de calidad: B. López-Hernández, A. Corma-Gómez, R. López-Sepúlveda, I. Capitán-del Río y M.D. Sánchez Mariscal. Análisis e interpretación de los datos: B. López-Hernández, A. Corma-Gómez e I. Capitán-del Río. Preparación del manuscrito: A. Corma-Gómez, R. López-Sepúlveda, I. Capitán-del Río y B. López-Hernández. Edición del manuscrito: B. López-Hernández, A. Corma-Gómez, R. López-Sepúlveda e I. Capitán-del Río. Revisión del manuscrito: la versión definitiva del artículo cuenta con la aprobación de todos/as los/las autores/as.
FinanciaciónNinguna.
Conflictos de interesesNinguno.
A Manuela Expósito Ruiz, Técnica de Metodología de la Investigación-Bioestadística de la Fundación para la Investigación Biosanitaria de Andalucía Oriental, por sus consejos en el análisis estadístico.